Biopolimeri- klasa polimera koji se prirodno nalaze u prirodi, a koji su dio živih organizama: proteini, nukleinske kiseline, polisaharidi. Biopolimeri se sastoje od identičnih (ili različitih) jedinica – monomera. Monomeri proteina - aminokiseline, nukleinske kiseline - nukleotidi, u polisaharidima - monosaharidi.
Postoje dvije vrste biopolimera – pravilni (neki polisaharidi) i nepravilni (proteini, nukleinske kiseline, neki polisaharidi).
Vjeverice
Proteini imaju nekoliko razina organizacije – primarnu, sekundarnu, tercijarnu, a ponekad i kvartarnu. Primarna struktura određena je slijedom monomera, dok je sekundarna struktura određena unutarmolekularnim i međumolekularnim interakcijama između monomera, obično pomoću vodikovih veza. Tercijarna struktura ovisi o interakciji sekundarnih struktura, kvaternar, u pravilu, nastaje kombiniranjem nekoliko molekula s tercijarnom strukturom.
Sekundarna struktura proteina nastaje međudjelovanjem aminokiselina preko vodikovih veza i hidrofobnih međudjelovanja. Glavni tipovi sekundarne strukture su
α-heliks, kada se javljaju vodikove veze između aminokiselina u istom lancu,
β-listovi (presavijeni slojevi), kada se stvaraju vodikove veze između različitih polipeptidnih lanaca koji idu u različitim smjerovima (antiparalelni,
neuređena područja
Za predviđanje sekundarne strukture koriste se računalni programi.
Tercijarna struktura ili "nabor" nastaje međudjelovanjem sekundarnih struktura i stabilizira se nekovalentnim, ionskim, vodikovim vezama i hidrofobnim interakcijama. Proteini koji obavljaju slične funkcije obično imaju sličnu tercijarnu strukturu. Primjer preklopa je β-bačva (bačva), kada su β-listovi raspoređeni u krug. Tercijarna struktura proteina određena je analizom rendgenske difrakcije.
Važna klasa polimernih proteina su fibrilarni proteini, od kojih je najpoznatiji kolagen.
U životinjskom svijetu proteini obično djeluju kao potpora, polimer koji stvara strukturu. Ovi polimeri su izgrađeni od 20 α-aminokiselina. Aminokiselinski ostaci povezani su u proteinske makromolekule peptidnim vezama koje nastaju reakcijom karboksilnih i amino skupina.
Važnost proteina u divljini ne može se precijeniti. Ovo je građevni materijal živih organizama, biokatalizatora - enzima koji osiguravaju tijek reakcija u stanicama i enzima koji potiču određene biokemijske reakcije, tj. osigurava selektivnost biokatalize. Naši mišići, kosa, koža sastoje se od vlaknastih proteina. Krvni protein, koji je dio hemoglobina, potiče apsorpciju atmosferskog kisika, drugi protein - inzulin - odgovoran je za razgradnju šećera u tijelu i, prema tome, za opskrbu energijom. Molekularna težina proteina jako varira. Tako inzulin, prvi od proteina čiju je strukturu utvrdio F. Sanger 1953. godine, sadrži oko 60 jedinica aminokiselina, a njegova molekularna težina je samo 12 000. Do danas je identificirano nekoliko tisuća proteinskih molekula, molekularna težina nekih od njih doseže 106 ili više.
Nukleinske kiseline
Primarna struktura DNA je linearni niz nukleotida u lancu. Redoslijed se u pravilu piše u obliku slova (npr. AGTCATGCCAG), a snimanje se vrši od 5" do 3" kraja lanca.
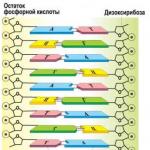
Sekundarna struktura je struktura nastala zbog nekovalentnih interakcija nukleotida (uglavnom dušičnih baza) međusobno, slaganja i vodikovih veza. Dvostruka spirala DNA je klasičan primjer sekundarne strukture. Ovo je najčešći oblik DNA u prirodi, koji se sastoji od dva antiparalelna komplementarna polinukleotidna lanca. Antiparalelizam se provodi zbog polariteta svakog od krugova. Komplementarnost se razumijeva kao podudarnost svakoj dušičnoj bazi jednog lanca DNA sa strogo definiranom bazom drugog lanca (nasuprot A je T, a nasuprot G je C). DNK se drži u dvostrukoj spirali komplementarnim sparivanjem baza – stvaranjem vodikovih veza, dvije u A-T paru i tri u G-C paru.
Godine 1868. švicarski znanstvenik Friedrich Miescher izolirao je tvar koja sadrži fosfor iz jezgri stanica koju je nazvao nuklein. Kasnije su te i slične tvari nazvane nukleinske kiseline. Njihova molekularna težina može doseći 109, ali češće se kreće od 105-106. Polazne tvari od kojih su izgrađeni nukleotidi – karike makromolekula nukleinskih kiselina su: ugljikohidrati, fosforna kiselina, purinske i pirimidinske baze. U jednoj skupini kiselina, riboza djeluje kao ugljikohidrat, u drugoj - deoksiriboza.
U skladu s prirodom ugljikohidrata koji ulaze u njihov sastav, nukleinske kiseline se nazivaju ribonukleinske i deoksiribonukleinske kiseline. Uobičajene kratice su RNA i DNA. Nukleinske kiseline imaju najvažniju ulogu u životnim procesima. Uz njihovu pomoć rješavaju se dva najvažnija zadatka: pohranjivanje i prijenos nasljednih informacija i matrična sinteza DNA, RNA i proteinskih makromolekula.
polisaharidi
3D struktura celuloze
Polisaharidi koje sintetiziraju živi organizmi sastoje se od velikog broja monosaharida povezanih glikozidnim vezama. Često su polisaharidi netopljivi u vodi. To su obično vrlo velike, razgranate molekule. Primjeri polisaharida koje sintetiziraju živi organizmi su skladišne tvari škrob i glikogen, kao i strukturni polisaharidi - celuloza i hitin. Budući da su biološki polisaharidi sastavljeni od molekula različitih duljina, pojmovi sekundarne i tercijarne strukture ne odnose se na polisaharide.
Polisaharidi se formiraju od spojeva niske molekularne težine koji se nazivaju šećeri ili ugljikohidrati. Cikličke molekule monosaharida mogu se međusobno vezati stvaranjem tzv. glikozidnih veza kondenzacijom hidroksilnih skupina.
Najčešći polisaharidi, čije su jedinice koje se ponavljaju ostaci α-D-glukopiranoze ili njezinih derivata. Najpoznatija i široko korištena celuloza. Kod ovog polisaharida kisikov most povezuje 1. i 4. atom ugljika u susjednim jedinicama, takva veza se naziva α-1,4-glikozidna.
Kemijski sastav je sličan celulozi, škrobu, sastoji se od amiloze i amilopektina, glikogena i dekstrana. Razlika između prve i celuloze je u grananju makromolekula, a amilopektin i glikogen mogu se svrstati u hiperrazgranate prirodne polimere, tj. dendrimeri nepravilne strukture. Točka grananja je obično šesti atom ugljika α-D-glukopiranoznog prstena, koji je povezan glikozidnom vezom s bočnim lancem. Razlika između dekstrana i celuloze leži u prirodi glikozidnih veza - uz α-1,4-, dekstran sadrži i α-1,3- i α-1,6-glikozidne veze, pri čemu je potonja dominantna.
Hitin i hitozan imaju drugačiji kemijski sastav od celuloze, ali su joj po strukturi bliski. Razlika je u tome što je na drugom atomu ugljika α-D-glukopiranoznih jedinica povezanih α-1,4-glikozidnim vezama OH skupina zamijenjena skupinama –NHCH3COO u hitinu i –NH2 skupinom u hitozanu.
Celuloza se nalazi u kori i drvu drveća, stabljikama biljaka: pamuk sadrži više od 90% celuloze, crnogorično drveće - preko 60%, listopadno - oko 40%. Čvrstoća celuloznih vlakana je zbog činjenice da su formirana od pojedinačnih kristala u kojima su makromolekule pakirane paralelno jedna uz drugu. Celuloza je strukturna osnova predstavnika ne samo biljnog svijeta, već i nekih bakterija.
U životinjskom svijetu polisaharide "koriste" samo kukci i člankonošci kao potporne polimere koji tvore strukturu. Najčešće se u te svrhe koristi hitin koji služi za izgradnju takozvanog vanjskog kostura kod rakova, rakova i škampa. Iz hitina deacetilacijom dobiva se kitozan koji je za razliku od netopljivog hitina topiv u vodenim otopinama mravlje, octene i klorovodične kiseline. U tom pogledu, a također i zbog kompleksa vrijednih svojstava u kombinaciji s biokompatibilnošću, kitozan ima velike izglede za široku praktičnu primjenu u skoroj budućnosti.
Škrob je jedan od polisaharida koji u biljkama djeluje kao rezervno hranjivo. Gomolji, plodovi, sjemenke sadrže do 70% škroba. Pohranjeni polisaharid životinja je glikogen, koji se uglavnom nalazi u jetri i mišićima.
Čvrstoću debla i stabljike biljaka, osim skeleta od celuloznih vlakana, određuje vezivno biljno tkivo. Značajan dio u drveću je lignin - do 30%. Njegova struktura nije točno utvrđena. Poznato je da se radi o hiperrazgranatom polimeru relativno niske molekulske mase (M ≈ 104), koji se uglavnom sastoji od fenolnih ostataka supstituiranih –OCH3 skupinama u orto položaju i –CH=CH–CH2OH skupinama u para položaju. Trenutno je velika količina lignina akumulirana kao otpad iz industrije hidrolize celuloze, ali problem njihovog zbrinjavanja nije riješen. Potporni elementi biljnog tkiva uključuju pektinske tvari, a posebno pektin koji se nalazi uglavnom u staničnoj stijenci. Njegov sadržaj u kori jabuke i bijelom dijelu kore agruma doseže 30%. Pektin spada u heteropolisaharide, tj. kopolimeri. Njegove makromolekule uglavnom su građene od ostataka D-galakturonske kiseline i njenog metil estera povezanih α-1,4-glikozidnim vezama.
Od pentoza su važni polimeri arabinoze i ksiloze koji tvore polisaharide koji se nazivaju arabini i ksilani. Oni, zajedno s celulozom, određuju tipična svojstva drva.
Nukleinske kiseline su prirodni organski visokomolekularni organski spojevi koji omogućuju pohranjivanje i prijenos nasljednih (genetskih) informacija u živim organizmima.
Nukleinske kiseline su DNA (dezoksiribonukleinska kiselina) i RNA (ribonukleinska kiselina). Otkrio ih je 1869. F. Miescher u jezgrama leukocita i nazvao ih nukleinskim, jer. nukleus – jezgra (nukleus).
Biopolimer čiji je monomer nukleotid. DNA je polinukleotid s vrlo velikom molekulskom težinom. Jedna molekula može sadržavati 10 8 ili više nukleotida. Nukleotid se sastoji od šećera deoksiriboze od pet atoma, ostatka fosforne kiseline i jedne dušične baze. Postoje samo četiri dušične baze - adenin (A), gvanin (G), citozin (C) i timin (T). Dakle, postoje samo četiri nukleotida: adenin, gvanin, citozin i timin (slika 10).

Riža. 10. Shema strukture DNA. 11. Struktura dijela molekule DNA
 Redoslijed nukleotida u DNK razlikuje se od organizma do organizma.
Redoslijed nukleotida u DNK razlikuje se od organizma do organizma.
Godine 1953. D. Watson i F. Crick izgradili su prostorni model DNK. Ovom su otkriću pridonijela dva eksperimentalna napretka:
1) Chargaff je primio čiste uzorke DNK i analizirao broj baza u svakom uzorku. Pokazalo se da bez obzira iz kojeg je organizma DNK izolirana, količina adenina jednaka je količini timina ( A = T), a količina gvanina jednaka je količini citozina ( G = C);
2) Wilkins i Franklin su pomoću X-zraka dobili dobru sliku DNK (slika 12).
Molekula DNA sastoji se od dva međusobno povezana lanca i izgleda kao ljestve od užeta (slika 11). Bočne strane stepenica su uvijene poput električnih žica. Strane su naizmjenični šećer i fosforna kiselina. Prečke ove ljestvice su dušične baze povezane prema principu komplementarnosti (A \u003d T; G \u003d C). Između adenina i timina postoji dvostruka vodikova veza, a između gvanina i citozina trostruka vodikova veza.

Riža. 13 Struktura nukleotida
Širina dvostruke spirale je 1,7 nm, jedan zavoj uključuje 10 parova baza, duljina zavoja je 3,4 nm, udaljenost između nukleotida je 0,34 nm. U kombinaciji s određenim proteinima - histonima - povećava se stupanj spiralizacije molekule. Molekula se zgušnjava i skraćuje. U budućnosti spiralizacija doseže maksimum, nastaje spirala još više razine - super spirala. U tom slučaju, molekula postaje vidljiva u svjetlosnom mikroskopu kao izduženo, dobro obojeno tijelo - kromosom.
sinteza DNA
DNA je dio kromosoma (kompleks DNA s proteinom histonom čini 90% kromosoma. Postavlja se pitanje zašto se nakon diobe stanice broj kromosoma ne smanjuje, nego ostaje isti. Jer prije diobe stanice dolazi do udvostručenja. javlja se (sinteza) DNK, a posljedično i udvostručenje kromosoma. Pod utjecajem enzima nukleaze dolazi do prekida vodikovih veza između dušičnih baza u određenom dijelu DNA i dvostruki lanac DNA počinje se odmotavati, jedan lanac se odmiče od drugog. Od slobodnih nukleotida koji se pod djelovanjem enzima nalaze u jezgri stanice DNA polimeraza grade se komplementarni filamenti. Svaki od razdvojenih parnih lanaca molekule DNA služi kao matrica za formiranje drugog komplementarnog lanca oko njega. Zatim se svaka stara (majčina) i nova (kćeri) nit ponovno uvijaju u obliku spirale. Kao rezultat toga nastaju dvije nove potpuno identične dvostruke spirale (slika 14).
Sposobnost reprodukcije vrlo je važna značajka molekule DNA.
Riža. 14. "Majčina" DNK služi kao obrazac za sintezu komplementarnih niti
Funkcija DNA u stanici
Dezoksiribonukleinska kiselina obavlja iznimno važne funkcije potrebne kako za održavanje tako i za reprodukciju života.
Prvo , - Ovaj pohranjivanje nasljednih informacija, koji je zatvoren u nukleotidnom nizu jednog od njegovih lanaca. Najmanja jedinica genetske informacije nakon nukleotida su tri uzastopna nukleotida. trojka. Redoslijed tripleta u polinukleotidnom lancu određuje redoslijed aminokiselina u proteinskoj molekuli. Trojke smještene jedna za drugom, koje određuju strukturu jednog polipeptidnog lanca su gen.
Druga funkcija DNK je prijenos nasljednih informacija s koljena na koljeno. Provodi se zahvaljujući reduplikacija(udvostručenje) roditeljske molekule i naknadna raspodjela molekula kćeri između stanica – potomaka. To je dvolančana struktura molekula DNA koja određuje mogućnost stvaranja apsolutno identičnih molekula kćeri tijekom reduplikacije.
Konačno, DNK je uključena kao predložak u procesu prijenosa genetskih informacija iz jezgre u citoplazmu do mjesta sinteze proteina. Istodobno se na jednom od njegovih lanaca, prema principu komplementarnosti, sintetizira molekula glasničke RNK iz nukleotida okoline koja molekulu okružuje.
RNA je, kao i DNA, biopolimer (polinukleotid) čiji su monomeri nukleotidi (slika 15). Dušične baze triju nukleotida iste su kao one koje čine DNA (adenin, gvanin, citozin), četvrti - uracil- prisutan je u molekuli RNA umjesto timina. RNA nukleotidi sadrže različite pentoze - riboza(umjesto deoksiriboze). Prema strukturi razlikuju se dvolančane i jednolančane RNA. Dvolančane RNA čuvari su genetske informacije u brojnim virusima, tj. obavljaju funkcije kromosoma.
RNA nose informacije o redoslijedu aminokiselina u proteinima, tj. o građi proteina, od kromosoma do mjesta njihove sinteze, te sudjeluju u sintezi proteina.
Postoji nekoliko tipova jednolančane RNK. Njihova imena određena su njihovom funkcijom i mjestom u stanici. Sve vrste RNK sintetizirane su na DNK, koja služi kao predložak.
 1. Prijenosna RNA(t-RNA) Najmanji, sastoji se od 76 - 85 nukleotida. Izgleda kao list djeteline na čijem se dugom kraju nalazi triplet nukleotida (ACC) na koji je vezana aktivirana aminokiselina.Na kraćem kraju je dušična baza – gvanin, sprječava uništavanje t-RNA. . Na suprotnom kraju je antikodon, koji je strogo komplementaran genetskom kodu na messenger RNA. Glavna funkcija tRNA je prijenos aminokiselina do mjesta sinteze proteina. Od ukupnog sadržaja RNA u stanici, tRNA čini 10%.
1. Prijenosna RNA(t-RNA) Najmanji, sastoji se od 76 - 85 nukleotida. Izgleda kao list djeteline na čijem se dugom kraju nalazi triplet nukleotida (ACC) na koji je vezana aktivirana aminokiselina.Na kraćem kraju je dušična baza – gvanin, sprječava uništavanje t-RNA. . Na suprotnom kraju je antikodon, koji je strogo komplementaran genetskom kodu na messenger RNA. Glavna funkcija tRNA je prijenos aminokiselina do mjesta sinteze proteina. Od ukupnog sadržaja RNA u stanici, tRNA čini 10%.
2. Ribosomska RNA(r-RNA) sadržane u ribosomima, sastoje se od 3 - 5 tisuća nukleotida. Od ukupnog sadržaja RNK u stanici, rRNA čini 90%.
3. Informacijska (i-RNA) ili matrična (m-RNA) . Sadržane u jezgri i citoplazmi, molekule messenger RNA mogu se sastojati od 300 - 30 000 nukleotida. Njegova funkcija je prijenos informacija o primarnoj strukturi proteina do ribosoma. Udio i-RNA čini 0,5 - 1% ukupnog sadržaja RNA u stanici.
Genetski kod
Genetski kod- ovo je sustav za bilježenje informacija o slijedu aminokiselina u proteinima pomoću slijeda nukleotida u DNA (slika 16).

Sl.16 Genetski kod
Svojstva genetskog koda
1. trostruki kod. To znači da je svaka od aminokiselina kodirana nizom od tri nukleotida tzv triplet ili kodon. Dakle, aminokiselina cistein odgovara tripletu ACA, valin CAA, a lizin TTT (slika).
2Kod je degeneriran. Ukupno ima 64 genetska koda, dok je 20 aminokiselina kodirano, kada one odu u mRNA, sinteza proteina prestaje. Svaka aminokiselina je kodirana s nekoliko genetskih kodova, s izuzetkom metionina i triptofana. Ovaj redundantnost koda od velike je važnosti za povećanje pouzdanosti prijenosa genetske informacije. Na primjer, aminokiselina arginin može odgovarati tripletima HCA, HCT, HCC itd. Jasno je da nasumična zamjena trećeg nukleotida u tim tripletima neće ni na koji način utjecati na strukturu sintetiziranog proteina.
3. Šifra je univerzalna. Genetski kod je isti za sva bića koja žive na Zemlji (za ljude, životinje, biljke, bakterije i gljive).
4. Genetski kod je kontinuiran. Nukleotidi u DNK se ne preklapaju, između tripleta (kodona) nema razmaka ni interpunkcijskih znakova. Kako je onda dio molekule DNA koji nosi informaciju o strukturi jednog proteina odijeljen od ostalih dijelova? Postoje tripleti čija je funkcija pokretanje sinteze polinukleotidnog lanca i tripleti ( UAA, UAG, UGA) koji zaustavljaju sintezu.
5. Genetski kod je specifičan. Ne postoje slučajevi kada bi isti triplet odgovarao više od jedne aminokiseline.
Biosinteza proteina u stanici
Biosinteza proteina u stanici sastoji se od dvije faze:
1. Transkripcija.
2. Emitiranje.
1. Transkripcija - To je prepisivanje informacija o primarnoj strukturi proteina iz određene DNA regije (gena) u i-RNA prema principu komplementarnosti uz pomoć enzima RNA polimeraze.
Čitanje nasljednih informacija započinje određenim dijelom DNK, koji se naziva promotor. Nalazi se prije gena i uključuje oko 80 nukleotida. RNK enzim – polimeraza prepoznaje promotor, čvrsto se veže za njega i topi ga, odvajajući nukleotide komplementarnih lanaca DNK, tada ovaj enzim počinje
 kreću se duž gena i, kako su DNA lanci odspojeni, mRNA se sintetizira na jednom od njih, koji se naziva osjetilni lanac. Gotova mRNA ulazi u citoplazmu kroz pore nuklearne ovojnice i prodire u malu podjedinicu ribosoma, a oni dijelovi gena na kojima je polimeraza formirala mRNA ponovno se uvijaju u spiralu, mRNA može prodrijeti u nekoliko ribosoma odjednom , a ovaj kompleks se zove polisoma. U citoplazmi se aminokiseline aktiviraju pomoću enzima aminoacil-t-sintetaze i pričvršćuju se na dugi kraj t-RNA (slika 17). 2. Translacija je prevođenje nasljedne informacije s jezika nukleotida na jezik aminokiselina.
kreću se duž gena i, kako su DNA lanci odspojeni, mRNA se sintetizira na jednom od njih, koji se naziva osjetilni lanac. Gotova mRNA ulazi u citoplazmu kroz pore nuklearne ovojnice i prodire u malu podjedinicu ribosoma, a oni dijelovi gena na kojima je polimeraza formirala mRNA ponovno se uvijaju u spiralu, mRNA može prodrijeti u nekoliko ribosoma odjednom , a ovaj kompleks se zove polisoma. U citoplazmi se aminokiseline aktiviraju pomoću enzima aminoacil-t-sintetaze i pričvršćuju se na dugi kraj t-RNA (slika 17). 2. Translacija je prevođenje nasljedne informacije s jezika nukleotida na jezik aminokiselina.
Translacija počinje s početnim kodonom AUG, na koji je t-RNA napunjena metioninom pričvršćena svojim UAC antikodonom. Velika podjedinica ribosoma sadrži aminoacil i peptidil središta. Najprije aminokiselina I (metionin) ulazi u aminoacilni centar, a zatim zajedno sa svojom t-RNA prelazi u peptidilni centar. Aminoacil centar se oslobađa i može prihvatiti sljedeću tRNA sa svojom aminokiselinom. Druga tRNA, napunjena drugom aminokiselinom, ulazi u veliku podjedinicu ribosoma i povezuje se sa svojim komplementarnim kodonom mRNA sa svojim antikodonom. Odmah se uz pomoć enzima peptidil transferaze prethodna aminokiselina svojom karboksilnom skupinom (COOH) povezuje s amino skupinom (NH 2) novopridošle aminokiseline. Između njih nastaje peptidna veza (-CO-NH-). Kao rezultat toga, t-RNA koja je donijela metionin se oslobađa, a dvije aminokiseline (dipeptid) se vežu na t-RNA u aminoacilnom centru. Za daljnji proces rasta polipeptidnog lanca potrebno je oslobađanje aminoacilnog centra. Velika i mala podjedinica ribosoma pomiču se jedna u odnosu na drugu (poput sata na navijanje), triplet nukleotida na mRNA pomiče se naprijed, a sljedeći triplet nukleotida zauzima njegovo mjesto. Sukladno kodonu i-RNA, sljedeća t-RNA dovodi aminokiselinu u oslobođeni aminoacilni centar, koji je s prethodnim povezan peptidnom vezom, a druga t-RNA napušta ribosom. Zatim ribosom ponovno napreduje za jedan kodon i proces se ponavlja. Postoji sekvencijalno pričvršćivanje aminokiselina na polipeptidni lanac u strogom skladu sa slijedom stupaca na mRNA.
Prezentacija na temu: Viši prirodni polimeri – Proteini i Nukleinske kiseline

























1 od 25
Prezentacija na temu:
slajd broj 1

Opis slajda:
slajd broj 2

Opis slajda:
Svrha sata: Učvrstiti i produbiti razumijevanje učenika o prirodnim polimerima na primjeru proteina i nukleinskih kiselina. Usustaviti znanja o sastavu, strukturi, svojstvima i funkcijama proteina. Imati predodžbu o kemijskoj i biološkoj sintezi bjelančevina, stvaranju umjetne i sintetičke hrane. Proširiti razumijevanje sastava i strukture nukleinskih kiselina. Znati objasniti konstrukciju dvostruke spirale DNA prema principu komplementarnosti. Poznavati ulogu nukleinskih kiselina u životu organizama. Nastavite razvijati vještine samoobrazovanja, sposobnost slušanja predavanja, isticanje glavne stvari. Voditi bilješke o izradi plana ili teza. Razvijati spoznajni interes učenika, uspostavljati međupredmetno povezivanje (s biologijom).
slajd broj 3

Opis slajda:
slajd broj 4

Opis slajda:
slajd broj 5

Opis slajda:
Vrijednosti proteina Sastav organizama koji danas žive na Zemlji sadrži oko tisuću milijardi tona proteina. Odlikujući se neiscrpnom raznolikošću strukture, koja je ujedno strogo specifična za svaku od njih, proteini stvaraju, zajedno s nukleinskim kiselinama, materijalnu osnovu za postojanje sveg bogatstva organizama svijeta koji nas okružuje. Proteine karakterizira sposobnost intramolekulskih interakcija, zbog čega je struktura tako dinamična, a oblik proteinskih molekula promjenjiv. Proteini su u interakciji s različitim tvarima. Spajajući se međusobno ili s nukleinskim kiselinama, polisaharidima i lipidima, tvore ribosome, mitohondrije, lizosome, membrane endoplazmatskog retikuluma i druge substanične strukture u kojima se odvijaju različiti metabolički procesi. Dakle, proteini igraju izuzetnu ulogu u fenomenima života.
slajd broj 6

Opis slajda:
Razine organizacije proteinske molekule Primarna Sekundarna Tercijarna Kvartarna Jedan od teških zadataka proteinske kemije bio je dešifrirati slijed aminokiselinskih ostataka u polipeptidnom lancu, odnosno primarnu strukturu proteinske molekule. Prvi ga je riješio engleski znanstvenik F. Sanger sa suradnicima 1945.-1956. Utvrdili su primarnu strukturu hormona inzulina, proteina koji proizvodi gušterača. Za to je F. Sanger 1958. godine dobio Nobelovu nagradu.
slajd broj 7

Opis slajda:
slajd broj 8

Opis slajda:
slajd broj 9

Opis slajda:
slajd broj 10

Opis slajda:
Kemijska svojstva proteina (video film) Karakteristična reakcija proteina – denaturacija: Koagulacija proteina zagrijavanjem.Taloženje proteina koncentriranim alkoholom.Taloženje proteina solima teških metala.2. Obojene reakcije proteina: Ksantoproteinska reakcija Biuretska reakcija Određivanje sadržaja sumpora u proteinskoj molekuli.
slajd broj 11

Opis slajda:
Uloga proteina u procesima vitalne aktivnosti Od velikog je interesa proučavanje ne samo strukture, već i uloge proteina u procesima vitalne aktivnosti. Mnogi od njih imaju zaštitna (imunoglobulini) i toksična (zmijski otrovi, toksini kolere, difterije i tetanusa, enterotoksin B iz staphylococcus aureusa, toksin butulizma) značajna za medicinske svrhe. Ali najvažnije je da su bjelančevine najvažniji i nezamjenjivi dio ljudske prehrane. U naše vrijeme 10-15% svjetske populacije gladuje, a 40% prima nezdravu hranu s nedovoljno proteina. Stoga je čovječanstvo prisiljeno proizvoditi proteine industrijskim putem - najoskudniji proizvod na Zemlji. Ovaj problem se intenzivno rješava na tri načina: proizvodnjom stočnog kvasca, tvorničkim pripremanjem proteinsko-vitaminskih koncentrata na bazi naftnih ugljikovodika i izdvajanjem proteina iz neprehrambenih sirovina biljnog podrijetla. Kod nas se od ugljikovodičnih sirovina proizvodi proteinsko-vitaminski koncentrat. Industrijska proizvodnja esencijalnih aminokiselina također je obećavajuća kao zamjena za proteine. Poznavanje strukture i funkcija proteina približava čovječanstvo svladavanju najskrovitije tajne samog fenomena života.
slajd broj 12

Opis slajda:
NUKLEINSKE KISELINE Nukleinske kiseline - prirodni visokomolekularni organski spojevi, polinukleotidi, osiguravaju pohranjivanje i prijenos nasljednih (genetskih) informacija u živim organizmima. Nukleinske kiseline otkrio je 1869. godine švicarski znanstvenik F. Miescher kao sastavni dio staničnih jezgri, pa su ime dobile po latinskoj riječi nucleus - jezgra. Nycleus ”- jezgra. Po prvi put DNA i RNA ekstrahirane su iz jezgre stanice. Stoga se nazivaju nukleinske kiseline. Građu i funkcije nukleinskih kiselina proučavali su američki biolog J. Watson i engleski fizičar F. Crick.
slajd broj 13

Opis slajda:
Godine 1953. američki biokemičar J. Watson i engleski fizičar F. Crick izgradili su model prostorne strukture DNK; koji izgleda kao dvostruka spirala. To je odgovaralo podacima engleskih znanstvenika R. Franklina i M. Wilkinsa, koji su pomoću rendgenske difrakcijske analize DNK uspjeli odrediti opće parametre spirale, njezin promjer i udaljenost između zavoja. Godine 1962. Watson, Crick i Wilkins dobili su Nobelovu nagradu za ovo važno otkriće.
slajd broj 14

Opis slajda:
slajd broj 15

Opis slajda:
Struktura nukleinskih kiselina Postoje tri vrste nukleinskih kiselina: DNA (dezoksiribonukleinske kiseline), RNA (ribonukleinske kiseline) i ATP (adenozin trifosfat). Poput ugljikohidrata i proteina, oni su polimeri. Kao i proteini, nukleinske kiseline su linearni polimeri. Međutim, njihovi monomeri - nukleotidi - složene su tvari, za razliku od prilično jednostavnih šećera i aminokiselina.
slajd broj 16

Opis slajda:
Usporedne karakteristike DNA i RNA DNA Biološki polimer Monomer – nukleotid 4 vrste dušičnih baza: adenin, timin, gvanin, citozin Komplementarni parovi: adenin-timin, gvanin-citozin Položaj – jezgra Funkcije – pohranjivanje nasljednih informacija Šećer – deoksiriboza RNA Biološki polimer Monomer - nukleotid 4 vrste dušičnih baza: adenin, gvanin, citozin, uracil Komplementarni parovi: adenin-uracil, gvanin-citozin Položaj - jezgra, citoplazma Funkcije - prijenos, prijenos nasljednih informacija Šećer - riboza Opis slajda:
slajd broj 23

Opis slajda:
Korištenje NC Tijekom života, osoba se razboli, uđe u nepovoljne proizvodne ili klimatske uvjete. Posljedica toga je povećanje "kvarova" u dobro funkcionirajućem genetskom aparatu. Do određenog vremena "neuspjesi" se ne manifestiraju prema van i mi ih ne primjećujemo. Jao! S vremenom promjene postaju vidljive. Prije svega, pojavljuju se na koži.Trenutno rezultati istraživanja biomakromolekula izlaze iz zidova laboratorija, počinjući aktivnije pomagati liječnicima i kozmetolozima u njihovom svakodnevnom radu. Davnih 1960-ih. postalo je poznato da izolirani lanci DNA uzrokuju regeneraciju stanica. Ali tek u zadnjim godinama 20. stoljeća postalo je moguće koristiti ovo svojstvo za obnavljanje stanica kože koje stare.
slajd broj 24

Opis slajda:
Primjena NC znanosti još je daleko od mogućnosti korištenja egzogenih DNK niti (s izuzetkom virusne DNK) kao predloška za "novu" DNK sintezu izravno u ljudskim, životinjskim ili biljnim stanicama. Činjenica je da je stanica domaćina pouzdano zaštićena od uvođenja strane DNA pomoću specifičnih enzima prisutnih u njoj - nukleaza. Strana DNA će neizbježno proći kroz uništenje ili restrikciju pod djelovanjem nukleaza. DNA će biti prepoznata kao "strana" po odsutnosti u njoj specifičnog obrasca raspodjele metiliranih baza svojstvenih DNA stanice domaćina za svaki organizam. Pritom, što je bliži odnos stanica, to će njihov DNK više formirati hibride.Rezultat ovog istraživanja su razne kozmetičke kreme koje sadrže “čarobne niti” za pomlađivanje kože.
slajd broj 25

Opis slajda:
Učvršćivanje lekcije (kontrolni test) Mogućnost 11. Dvostruki polinukleotidni lanac karakterističan je za molekule: a) DNA b) RNAv) oba prethodna odgovora su točna.2. Prosječna molekularna težina, koja vrsta nukleinskih kiselina je veća? a) DNA b) RNA c) ovisi o vrsti žive stanice3. Koje tvari nisu sastavni dio nukleotida a) pirimidinska ili purinska baza b) riboza i deoksiriboza c) α-aminokiseline d) fosforna kiselina DNA nukleotidi ne sadrže sljedeće ostatke kao baze: a) citozin c) guaninab) uracil d) adenin e) timin5. Nukleotidni niz je struktura nukleinskih kiselina: a) primarne c) tercijarne b) sekundarne d) kvaterne 2 opcija1. Nukleinske kiseline dobile su naziv po latinskoj riječi: a) jezgra c) život b) stanica d) prva2. Polimerni lanac, koja od nukleinskih kiselina je niz nukleotida?a) DNA b) RNA c) obje vrste nukleinskih kiselina3. Sekundarna struktura u obliku dvostruke spirale karakteristična je za molekule: a) DNA c) RNAb) proteina d) svih nukleinskih kiselina4. Purinska baza nije: a) adenin c) gvanin b) timin d) svi su5. Molekula nukleotida ne sadrži: a) ostatak monosaharida c) ostatak dušične baze b) ostatak aminokiseline d) ostatak fosforne kiseline
Većina modernih građevinskih materijala, lijekova, tkanina, predmeta za kućanstvo, ambalaže i potrošnog materijala su polimeri. Ovo je cijela skupina spojeva koji imaju karakteristične karakteristike razlikovanja. Ima ih puno, ali unatoč tome, broj polimera i dalje raste. Uostalom, sintetički kemičari svake godine otkrivaju sve više i više novih tvari. U isto vrijeme, prirodni polimer je bio od posebne važnosti u svakom trenutku. Koje su to nevjerojatne molekule? Koja su njihova svojstva i koje su karakteristike? Odgovorit ćemo na ova pitanja u tijeku članka.
Polimeri: opće karakteristike
S gledišta kemije, polimer se smatra molekulom koja ima veliku molekularnu težinu: od nekoliko tisuća do milijuna jedinica. No, osim ove značajke, postoji još nekoliko po kojima se tvari mogu klasificirati upravo na prirodne i sintetske polimere. Ovaj:
- stalno ponavljajuće monomerne jedinice koje su povezane različitim interakcijama;
- stupanj polimeraze (tj. broj monomera) mora biti vrlo visok, inače će se spoj smatrati oligomerom;
- određena prostorna orijentacija makromolekule;
- skup važnih fizikalno-kemijskih svojstava koja su karakteristična samo za ovu skupinu.
Općenito, tvar polimerne prirode prilično je lako razlikovati od drugih. Dovoljno je samo pogledati njegovu formulu da bi se razumjela. Tipičan primjer je dobro poznati polietilen, široko korišten u svakodnevnom životu i industriji. To je proizvod u koji ulazi eten ili etilen. Opća reakcija je napisana na sljedeći način:
nCH 2 \u003d CH 2 → (-CH-CH-) n, gdje je n stupanj polimerizacije molekula, koji pokazuje koliko je monomernih jedinica uključeno u njegov sastav.
Također, kao primjer, može se navesti prirodni polimer, koji je svima dobro poznat, to je škrob. Osim toga, ovoj skupini spojeva pripadaju amilopektin, celuloza, pileći protein i mnoge druge tvari.
Reakcije, kao rezultat kojih se mogu formirati makromolekule, su dvije vrste:
- polimerizacija;
- polikondenzacija.
Razlika je u tome što su u drugom slučaju produkti interakcije niske molekularne težine. Struktura polimera može biti različita, ovisi o atomima koji ga tvore. Često postoje linearni oblici, ali postoje i trodimenzionalne mreže, vrlo složene.
Ako govorimo o silama i interakcijama koje drže monomerne jedinice zajedno, možemo identificirati nekoliko glavnih:
- Van der Waalsove sile;
- kemijske veze (kovalentne, ionske);
- elektrostatska interakcija.
Svi polimeri se ne mogu spojiti u jednu kategoriju, jer imaju potpuno drugačiju prirodu, način formiranja i obavljaju različite funkcije. Svojstva im se također razlikuju. Stoga postoji klasifikacija koja vam omogućuje da sve predstavnike ove skupine tvari podijelite u različite kategorije. Može se temeljiti na nekoliko značajki.

Klasifikacija polimera
Ako uzmemo kao osnovu kvalitativni sastav molekula, tada se sve tvari koje se razmatraju mogu podijeliti u tri skupine.
- Organski - to su oni koji uključuju atome ugljika, vodika, sumpora, kisika, fosfora, dušika. Odnosno oni elementi koji su biogeni. Primjeri uključuju puno: polietilen, polivinil klorid, polipropilen, viskoza, najlon, prirodni polimer - protein, nukleinske kiseline i tako dalje.
- Organski elementi - oni koji uključuju neku vrstu stranih anorganskih a ne Najčešće je to silicij, aluminij ili titan. Primjeri takvih makromolekula: stakleni polimeri, kompozitni materijali.
- Anorganski - lanac se temelji na atomima silicija, a ne na ugljiku. Radikali također mogu biti dio bočnih grana. Otkriveni su sasvim nedavno, sredinom 20. stoljeća. Koristi se u medicini, građevinarstvu, strojarstvu i drugim industrijama. Primjeri: silikon, cinober.
Ako polimere podijelimo prema podrijetlu, možemo razlikovati tri skupine.
- Prirodni polimeri, čija se uporaba naširoko provodi od antike. To su takve makromolekule, za čije stvaranje osoba nije uložila nikakve napore. Oni su proizvodi reakcija same prirode. Primjeri: svila, vuna, proteini, nukleinske kiseline, škrob, celuloza, koža, pamuk i drugi.
- Umjetna. To su makromolekule koje je stvorio čovjek, ali na temelju prirodnih analoga. Odnosno, svojstva već postojećeg prirodnog polimera jednostavno se poboljšavaju i mijenjaju. Primjeri: umjetni
- Sintetički - to su polimeri u čijem stvaranju sudjeluje samo osoba. Za njih nema prirodnih analoga. Znanstvenici razvijaju metode za sintezu novih materijala koji bi imali poboljšana tehnička svojstva. Tako nastaju sintetski polimerni spojevi raznih vrsta. Primjeri: polietilen, polipropilen, rajon itd.
Postoji još jedan znak koji je temelj podjele razmatranih tvari u skupine. To su reaktivnost i toplinska stabilnost. Postoje dvije kategorije za ovaj parametar:
- termoplastični;
- termoreaktivni.
Najstariji, najvažniji i posebno vrijedan još uvijek je prirodni polimer. Njegova svojstva su jedinstvena. Stoga ćemo dalje razmotriti ovu kategoriju makromolekula.

Koja tvar je prirodni polimer?
Da bismo odgovorili na ovo pitanje, pogledajmo prvo oko sebe. Što nas okružuje? Živi organizmi oko nas koji se hrane, dišu, razmnožavaju, cvjetaju i daju plodove i sjemenke. I što oni predstavljaju s molekularne točke gledišta? To su veze kao što su:
- bjelančevine;
- nukleinske kiseline;
- polisaharidi.
Dakle, svaki od gore navedenih spojeva je prirodni polimer. Dakle, ispada da život oko nas postoji samo zahvaljujući prisutnosti tih molekula. Ljudi su od davnina koristili glinu, građevne smjese i žbuke za učvršćivanje i stvaranje doma, tkali pređu od vune, a za izradu odjeće koristili pamuk, svilu, vunu i životinjsku kožu. Prirodni organski polimeri pratili su čovjeka u svim fazama njegova formiranja i razvoja te mu umnogome pomogli u postizanju rezultata koje danas imamo.
Sama priroda dala je sve kako bi život ljudi bio što ugodniji. S vremenom je guma otkrivena, razjašnjena su njena izvanredna svojstva. Čovjek je naučio koristiti škrob u prehrambene svrhe, a celulozu u tehničke svrhe. Kamfor je također prirodni polimer, što je također poznato od davnina. Smole, proteini, nukleinske kiseline su svi primjeri spojeva koji se razmatraju.
Struktura prirodnih polimera
Nisu svi predstavnici ove klase tvari raspoređeni na isti način. Dakle, prirodni i sintetski polimeri mogu se značajno razlikovati. Njihove molekule su usmjerene na takav način da je najkorisnije i najpovoljnije postojati s energetske točke gledišta. Istodobno, mnoge prirodne vrste mogu bubriti i njihova se struktura mijenja u procesu. Postoji nekoliko najčešćih opcija za strukturu lanca:
- linearni;
- razgranat;
- zvjezdasti;
- ravan;
- mreža;
- traka;
- češljastog oblika.
Umjetni i sintetski predstavnici makromolekula imaju vrlo veliku masu, ogroman broj atoma. Stvoreni su s posebno određenim svojstvima. Stoga je njihovu strukturu izvorno planirao čovjek. Prirodni polimeri najčešće su linearne ili mrežaste strukture.

Primjeri prirodnih makromolekula
Prirodni i umjetni polimeri vrlo su bliski jedni drugima. Uostalom, prvi postaju osnova za stvaranje drugog. Postoji mnogo primjera takvih transformacija. Pogledajmo neke od njih.
- Obična mliječno bijela plastika je proizvod dobiven obradom celuloze dušičnom kiselinom uz dodatak prirodnog kamfora. Reakcija polimerizacije uzrokuje skrućivanje rezultirajućeg polimera i postaje željeni proizvod. A plastifikator - kamfor, čini ga sposobnim da omekša kada se zagrije i promijeni svoj oblik.
- Acetatna svila, bakreno-amonijačno vlakno, viskoza - sve su to primjeri onih niti, vlakana koja se dobivaju na bazi celuloze. Lan i lanene tkanine nisu toliko izdržljive, ne sjaje se, lako se gužvaju. Ali umjetni analozi ovih nedostataka su lišeni, što njihovu upotrebu čini vrlo atraktivnom.
- Umjetno kamenje, građevinski materijali, mješavine, nadomjesci kože također su primjeri polimera dobivenih iz prirodnih sirovina.
Tvar, koja je prirodni polimer, također se može koristiti u svom pravom obliku. Ima i mnogo takvih primjera:
- kolofonij;
- jantar;
- škrob;
- amilopektin;
- celuloza;
- vuna;
- pamuk;
- svila;
- cement;
- glina;
- vapno;
- bjelančevine;
- nukleinske kiseline i tako dalje.
Očito je klasa spojeva koju razmatramo vrlo brojna, praktično važna i značajna za ljude. Sada pobliže pogledajmo nekoliko predstavnika prirodnih polimera koji su trenutno u velikoj potražnji.

Svila i vuna
Formula polimera prirodne svile je složena, jer je njegov kemijski sastav izražen sljedećim komponentama:
- fibroin;
- sericin;
- voskovi;
- masti.
Sam glavni protein, fibroin, u svom sastavu sadrži nekoliko vrsta aminokiselina. Ako zamislite njegov polipeptidni lanac, onda će izgledati otprilike ovako: (-NH-CH 2 -CO-NH-CH (CH 3) -CO-NH-CH 2 -CO-) n. A ovo je samo dio toga. Zamislimo li da je jednako složena molekula proteina sericina pričvršćena na tu strukturu uz pomoć van der Waalsovih sila, te su zajedno pomiješane u jedinstvenu konformaciju s voskom i mastima, onda je jasno zašto je teško prikazati formulu od prirodne svile.
Danas Kina isporučuje većinu ovog proizvoda, jer na njezinim otvorenim prostorima postoji prirodno stanište glavnog proizvođača - svilene bube. Ranije, počevši od najstarijih vremena, prirodna svila bila je visoko cijenjena. Samo su plemeniti, bogati ljudi mogli priuštiti odjeću od njega. Danas mnoge karakteristike ove tkanine ostavljaju mnogo za poželjeti. Na primjer, jako je magnetiziran i naboran, osim toga gubi sjaj i blijedi od izlaganja suncu. Stoga su više u upotrebi umjetni derivati koji se temelje na njemu.
Vuna je također prirodni polimer, budući da je otpadni proizvod kože i lojnih žlijezda životinja. Na temelju ovog proteinskog proizvoda izrađuje se pletivo, koje je, poput svile, vrijedan materijal.

Škrob
Prirodni polimer škrob je otpadni proizvod biljaka. Proizvode ga kao rezultat procesa fotosinteze i nakupljaju u različitim dijelovima tijela. Njegov kemijski sastav:
- amilopektin;
- amiloza;
- alfa glukoza.
Prostorna struktura škroba je vrlo razgranata, neuredna. Zahvaljujući amilopektinu koji je uključen u sastav, može nabubriti u vodi, pretvarajući se u takozvanu pastu. Ovaj se koristi u strojarstvu i industriji. Medicina, prehrambena industrija, proizvodnja ljepila za tapete također su područja primjene ove tvari.
Među biljkama koje sadrže maksimalnu količinu škroba, možemo razlikovati:
- kukuruz;
- krumpir;
- pšenica
- kasava;
- zob;
- heljda;
- banane;
- sirak.
Na temelju ovog biopolimera peče se kruh, izrađuje tjestenina, kuhaju se kiseljaci, žitarice i drugi prehrambeni proizvodi.

Celuloza
S gledišta kemije, ova tvar je polimer, čiji je sastav izražen formulom (C 6 H 5 O 5) n. Monomerna karika u lancu je beta-glukoza. Glavna mjesta sadržaja celuloze su stanične stijenke biljaka. Zato je drvo vrijedan izvor ovog spoja.
Celuloza je prirodni polimer linearne prostorne strukture. Koristi se za proizvodnju sljedećih vrsta proizvoda:
- proizvodi od celuloze i papira;
- umjetno krzno;
- razne vrste umjetnih vlakana;
- pamuk
- plastika;
- bezdimni prah;
- filmska vrpca i tako dalje.
Očito je njegova industrijska vrijednost velika. Da bi se određeni spoj mogao koristiti u proizvodnji, mora se prvo ekstrahirati iz biljaka. To se postiže dugotrajnim kuhanjem drva u posebnim uređajima. Daljnja obrada, kao i reagensi koji se koriste za probavu, variraju. Postoji nekoliko načina:
- sulfit;
- nitrat;
- soda;
- sulfat.
Nakon takve obrade proizvod još uvijek sadrži nečistoće. Temelji se na ligninu i hemicelulozi. Da bi ih se riješili, masa se tretira klorom ili alkalijom.
U ljudskom tijelu ne postoje takvi biološki katalizatori koji bi bili u stanju razgraditi ovaj složeni biopolimer. Međutim, neke životinje (biljojedi) su se tome prilagodile. Imaju određene bakterije u želucu koje to rade umjesto njih. Zauzvrat, mikroorganizmi dobivaju energiju za život i stanište. Ovakav oblik simbioze izuzetno je koristan za obje strane.

Guma
To je prirodni polimer od vrijedne ekonomske važnosti. Prvi ga je opisao Robert Cook, koji ga je otkrio na jednom od svojih putovanja. Desilo se ovako. Iskrcavši se na otok naseljen njemu nepoznatim domorocima, oni su ga gostoljubivo primili. Pozornost su mu privukla domaća djeca koja su se igrala neobičnim predmetom. Ovo kuglasto tijelo odgurnulo se od poda i odskočilo visoko uvis, a zatim se vratilo.
Upitavši lokalno stanovništvo od čega je napravljena ova igračka, Cook je saznao da se na taj način stvrdnjava sok jednog od stabala, hevee. Mnogo kasnije saznalo se da je riječ o gumenom biopolimeru.
Kemijska priroda ovog spoja je poznata - to je izopren koji je prošao prirodnu polimerizaciju. Formula gume (C 5 H 8) n. Njegova svojstva zbog kojih je tako visoko cijenjena su sljedeća:
- elastičnost;
- otpornost na habanje;
- električna izolacija;
- vodootporan.
Međutim, postoje i nedostaci. Na hladnoći postaje lomljiva i lomljiva, a na vrućini ljepljiva i viskozna. Zbog toga je postalo potrebno sintetizirati analoge umjetne ili sintetičke baze. Danas se gume široko koriste u tehničke i industrijske svrhe. Najvažniji proizvodi koji se temelje na njima:
- guma;
- eboniti.
jantar
Prirodni je polimer, jer je po svojoj strukturi smola, njen fosilni oblik. Prostorna struktura je okvirni amorfni polimer. Vrlo je zapaljivo i može se zapaliti plamenom šibice. Ima svojstva luminescencije. Ovo je vrlo važna i vrijedna kvaliteta koja se koristi u nakitu. Nakit na bazi jantara vrlo je lijep i tražen.
Osim toga, ovaj se biopolimer koristi i u medicinske svrhe. Od njega se također izrađuju brusni papir, lakovi za razne površine.
slajd 1
slajd 2
 Svrha sata: Učvrstiti i produbiti razumijevanje učenika o prirodnim polimerima na primjeru proteina i nukleinskih kiselina. Usustaviti znanja o sastavu, strukturi, svojstvima i funkcijama proteina. Imati predodžbu o kemijskoj i biološkoj sintezi bjelančevina, stvaranju umjetne i sintetičke hrane. Proširiti razumijevanje sastava i strukture nukleinskih kiselina. Znati objasniti konstrukciju dvostruke spirale DNA prema principu komplementarnosti. Poznavati ulogu nukleinskih kiselina u životu organizama. Nastavite razvijati vještine samoobrazovanja, sposobnost slušanja predavanja, isticanje glavne stvari. Voditi bilješke o izradi plana ili teza. Razvijati spoznajni interes učenika, uspostavljati međupredmetno povezivanje (s biologijom).
Svrha sata: Učvrstiti i produbiti razumijevanje učenika o prirodnim polimerima na primjeru proteina i nukleinskih kiselina. Usustaviti znanja o sastavu, strukturi, svojstvima i funkcijama proteina. Imati predodžbu o kemijskoj i biološkoj sintezi bjelančevina, stvaranju umjetne i sintetičke hrane. Proširiti razumijevanje sastava i strukture nukleinskih kiselina. Znati objasniti konstrukciju dvostruke spirale DNA prema principu komplementarnosti. Poznavati ulogu nukleinskih kiselina u životu organizama. Nastavite razvijati vještine samoobrazovanja, sposobnost slušanja predavanja, isticanje glavne stvari. Voditi bilješke o izradi plana ili teza. Razvijati spoznajni interes učenika, uspostavljati međupredmetno povezivanje (s biologijom).
slajd 3

slajd 4

slajd 5
 Vrijednosti proteina Sastav organizama koji danas žive na Zemlji sadrži oko tisuću milijardi tona proteina. Odlikujući se neiscrpnom raznolikošću strukture, koja je ujedno strogo specifična za svaku od njih, proteini stvaraju, zajedno s nukleinskim kiselinama, materijalnu osnovu za postojanje sveg bogatstva organizama svijeta koji nas okružuje. Proteine karakterizira sposobnost intramolekulskih interakcija, zbog čega je struktura tako dinamična, a oblik proteinskih molekula promjenjiv. Proteini su u interakciji s različitim tvarima. Spajajući se međusobno ili s nukleinskim kiselinama, polisaharidima i lipidima, tvore ribosome, mitohondrije, lizosome, membrane endoplazmatskog retikuluma i druge substanične strukture u kojima se odvijaju različiti metabolički procesi. Dakle, proteini igraju izuzetnu ulogu u fenomenima života.
Vrijednosti proteina Sastav organizama koji danas žive na Zemlji sadrži oko tisuću milijardi tona proteina. Odlikujući se neiscrpnom raznolikošću strukture, koja je ujedno strogo specifična za svaku od njih, proteini stvaraju, zajedno s nukleinskim kiselinama, materijalnu osnovu za postojanje sveg bogatstva organizama svijeta koji nas okružuje. Proteine karakterizira sposobnost intramolekulskih interakcija, zbog čega je struktura tako dinamična, a oblik proteinskih molekula promjenjiv. Proteini su u interakciji s različitim tvarima. Spajajući se međusobno ili s nukleinskim kiselinama, polisaharidima i lipidima, tvore ribosome, mitohondrije, lizosome, membrane endoplazmatskog retikuluma i druge substanične strukture u kojima se odvijaju različiti metabolički procesi. Dakle, proteini igraju izuzetnu ulogu u fenomenima života.
slajd 6
 Razine organizacije proteinske molekule Primarna Sekundarna Tercijarna Kvartarna Jedan od teških zadataka proteinske kemije bio je dešifrirati slijed aminokiselinskih ostataka u polipeptidnom lancu, odnosno primarnu strukturu proteinske molekule. Prvi ga je riješio engleski znanstvenik F. Sanger sa suradnicima 1945.-1956. Utvrdili su primarnu strukturu hormona inzulina, proteina koji proizvodi gušterača. Za to je F. Sanger 1958. godine dobio Nobelovu nagradu.
Razine organizacije proteinske molekule Primarna Sekundarna Tercijarna Kvartarna Jedan od teških zadataka proteinske kemije bio je dešifrirati slijed aminokiselinskih ostataka u polipeptidnom lancu, odnosno primarnu strukturu proteinske molekule. Prvi ga je riješio engleski znanstvenik F. Sanger sa suradnicima 1945.-1956. Utvrdili su primarnu strukturu hormona inzulina, proteina koji proizvodi gušterača. Za to je F. Sanger 1958. godine dobio Nobelovu nagradu.
Slajd 7
 specifičan slijed a-aminokiselinskih ostataka u polipeptidnom lancu Primarna struktura -
specifičan slijed a-aminokiselinskih ostataka u polipeptidnom lancu Primarna struktura -
Slajd 8

Slajd 9
 Kvartarna struktura - agregati nekoliko proteinskih makromolekula (proteinski kompleksi) nastali međudjelovanjem različitih polipeptidnih lanaca
Kvartarna struktura - agregati nekoliko proteinskih makromolekula (proteinski kompleksi) nastali međudjelovanjem različitih polipeptidnih lanaca
slajd 10
 Kemijska svojstva proteina (video film) Tipična reakcija proteina - denaturacija: Koagulacija proteina pri zagrijavanju. Taloženje proteina koncentriranim alkoholom. Taloženje proteina solima teških metala. 2. Obojene reakcije proteina: Ksantoproteinska reakcija Biuretska reakcija Određivanje sadržaja sumpora u proteinskoj molekuli.
Kemijska svojstva proteina (video film) Tipična reakcija proteina - denaturacija: Koagulacija proteina pri zagrijavanju. Taloženje proteina koncentriranim alkoholom. Taloženje proteina solima teških metala. 2. Obojene reakcije proteina: Ksantoproteinska reakcija Biuretska reakcija Određivanje sadržaja sumpora u proteinskoj molekuli.
slajd 11
 Uloga proteina u procesima vitalne aktivnosti Od velikog je interesa proučavanje ne samo strukture, već i uloge proteina u procesima vitalne aktivnosti. Mnogi od njih imaju zaštitna (imunoglobulini) i toksična (zmijski otrovi, toksini kolere, difterije i tetanusa, enterotoksin B iz staphylococcus aureusa, toksin butulizma) značajna za medicinske svrhe. Ali najvažnije je da su bjelančevine najvažniji i nezamjenjivi dio ljudske prehrane. U naše vrijeme 10-15% svjetske populacije gladuje, a 40% prima nezdravu hranu s nedovoljno proteina. Stoga je čovječanstvo prisiljeno proizvoditi proteine industrijskim putem - najoskudniji proizvod na Zemlji. Ovaj problem se intenzivno rješava na tri načina: proizvodnjom stočnog kvasca, tvorničkim pripremanjem proteinsko-vitaminskih koncentrata na bazi ugljikovodika ulja i izdvajanjem proteina iz neprehrambenih sirovina biljnog podrijetla. Kod nas se od ugljikovodičnih sirovina proizvodi proteinsko-vitaminski koncentrat. Industrijska proizvodnja esencijalnih aminokiselina također je obećavajuća kao zamjena za proteine. Poznavanje strukture i funkcija proteina približava čovječanstvo svladavanju najskrovitije tajne samog fenomena života.
Uloga proteina u procesima vitalne aktivnosti Od velikog je interesa proučavanje ne samo strukture, već i uloge proteina u procesima vitalne aktivnosti. Mnogi od njih imaju zaštitna (imunoglobulini) i toksična (zmijski otrovi, toksini kolere, difterije i tetanusa, enterotoksin B iz staphylococcus aureusa, toksin butulizma) značajna za medicinske svrhe. Ali najvažnije je da su bjelančevine najvažniji i nezamjenjivi dio ljudske prehrane. U naše vrijeme 10-15% svjetske populacije gladuje, a 40% prima nezdravu hranu s nedovoljno proteina. Stoga je čovječanstvo prisiljeno proizvoditi proteine industrijskim putem - najoskudniji proizvod na Zemlji. Ovaj problem se intenzivno rješava na tri načina: proizvodnjom stočnog kvasca, tvorničkim pripremanjem proteinsko-vitaminskih koncentrata na bazi ugljikovodika ulja i izdvajanjem proteina iz neprehrambenih sirovina biljnog podrijetla. Kod nas se od ugljikovodičnih sirovina proizvodi proteinsko-vitaminski koncentrat. Industrijska proizvodnja esencijalnih aminokiselina također je obećavajuća kao zamjena za proteine. Poznavanje strukture i funkcija proteina približava čovječanstvo svladavanju najskrovitije tajne samog fenomena života.
slajd 12
 NUKLEINSKE KISELINE Nukleinske kiseline - prirodni visokomolekularni organski spojevi, polinukleotidi, osiguravaju pohranjivanje i prijenos nasljednih (genetskih) informacija u živim organizmima. Nukleinske kiseline otkrio je 1869. godine švicarski znanstvenik F. Miescher kao sastavni dio staničnih jezgri, pa su ime dobile prema latinskoj riječi nucleus - jezgra. Nycleus" - jezgra. Po prvi put DNA i RNA ekstrahirane su iz jezgre stanice. Stoga se nazivaju nukleinske kiseline. Građu i funkcije nukleinskih kiselina proučavali su američki biolog J. Watson i engleski fizičar F. Crick.
NUKLEINSKE KISELINE Nukleinske kiseline - prirodni visokomolekularni organski spojevi, polinukleotidi, osiguravaju pohranjivanje i prijenos nasljednih (genetskih) informacija u živim organizmima. Nukleinske kiseline otkrio je 1869. godine švicarski znanstvenik F. Miescher kao sastavni dio staničnih jezgri, pa su ime dobile prema latinskoj riječi nucleus - jezgra. Nycleus" - jezgra. Po prvi put DNA i RNA ekstrahirane su iz jezgre stanice. Stoga se nazivaju nukleinske kiseline. Građu i funkcije nukleinskih kiselina proučavali su američki biolog J. Watson i engleski fizičar F. Crick.
slajd 13
 STRUKTURE DNK I RNK 1953. godine američki biokemičar J. Watson i engleski fizičar F. Crick konstruirali su model prostorne strukture DNK; koji izgleda kao dvostruka spirala. To je odgovaralo podacima engleskih znanstvenika R. Franklina i M. Wilkinsa, koji su pomoću rendgenske difrakcijske analize DNK uspjeli odrediti opće parametre spirale, njezin promjer i udaljenost između zavoja. Godine 1962. Watson, Crick i Wilkins dobili su Nobelovu nagradu za ovo važno otkriće.
STRUKTURE DNK I RNK 1953. godine američki biokemičar J. Watson i engleski fizičar F. Crick konstruirali su model prostorne strukture DNK; koji izgleda kao dvostruka spirala. To je odgovaralo podacima engleskih znanstvenika R. Franklina i M. Wilkinsa, koji su pomoću rendgenske difrakcijske analize DNK uspjeli odrediti opće parametre spirale, njezin promjer i udaljenost između zavoja. Godine 1962. Watson, Crick i Wilkins dobili su Nobelovu nagradu za ovo važno otkriće.
slajd 14
 NUKLEINSKE KISELINE MONOMERI - NUKLEOTID DNA - deoksiribonukleinska kiselina RNA ribonukleinska kiselina Sastav nukleotida u DNA Sastav nukleotida u RNA Dušične baze: Adenin (A) Gvanin (D) Citozin (C) Uracil (U): Riboza Ostatak fosforne kiseline Dušične baze: Adenin (A) ) Gvanin (G) Citozin (C) Timin (T) Dezoksiriboza Ostatak fosforne kiseline Messenger RNA (i-RNA) Prijenosna RNA (t-RNA) Ribosomska RNA (r-RNA)
NUKLEINSKE KISELINE MONOMERI - NUKLEOTID DNA - deoksiribonukleinska kiselina RNA ribonukleinska kiselina Sastav nukleotida u DNA Sastav nukleotida u RNA Dušične baze: Adenin (A) Gvanin (D) Citozin (C) Uracil (U): Riboza Ostatak fosforne kiseline Dušične baze: Adenin (A) ) Gvanin (G) Citozin (C) Timin (T) Dezoksiriboza Ostatak fosforne kiseline Messenger RNA (i-RNA) Prijenosna RNA (t-RNA) Ribosomska RNA (r-RNA)
slajd 15
 Postoje tri vrste nukleinskih kiselina: DNA (deoksiribonukleinske kiseline), RNA (ribonukleinske kiseline) i ATP (adenozin trifosfat). Poput ugljikohidrata i proteina, oni su polimeri. Kao i proteini, nukleinske kiseline su linearni polimeri. Međutim, njihovi monomeri - nukleotidi - složene su tvari, za razliku od prilično jednostavnih šećera i aminokiselina. Struktura nukleinskih kiselina
Postoje tri vrste nukleinskih kiselina: DNA (deoksiribonukleinske kiseline), RNA (ribonukleinske kiseline) i ATP (adenozin trifosfat). Poput ugljikohidrata i proteina, oni su polimeri. Kao i proteini, nukleinske kiseline su linearni polimeri. Međutim, njihovi monomeri - nukleotidi - složene su tvari, za razliku od prilično jednostavnih šećera i aminokiselina. Struktura nukleinskih kiselina
slajd 16
 Usporedne karakteristike DNA i RNA DNA Biološki polimer Monomer - nukleotid 4 vrste dušičnih baza: adenin, timin, gvanin, citozin. Komplementarni parovi: adenin-timin, gvanin-citozin Položaj - jezgra Funkcije - pohrana nasljednih informacija Šećer - deoksiriboza RNA Biološki polimer Monomer - nukleotid 4 vrste dušičnih baza: adenin, gvanin, citozin, uracil Komplementarni parovi: adenin-uracil, gvanin- citozin Mjesto – jezgra, citoplazma Funkcije – prijenos, prijenos nasljednih informacija. Šećer - riboza
Usporedne karakteristike DNA i RNA DNA Biološki polimer Monomer - nukleotid 4 vrste dušičnih baza: adenin, timin, gvanin, citozin. Komplementarni parovi: adenin-timin, gvanin-citozin Položaj - jezgra Funkcije - pohrana nasljednih informacija Šećer - deoksiriboza RNA Biološki polimer Monomer - nukleotid 4 vrste dušičnih baza: adenin, gvanin, citozin, uracil Komplementarni parovi: adenin-uracil, gvanin- citozin Mjesto – jezgra, citoplazma Funkcije – prijenos, prijenos nasljednih informacija. Šećer - riboza
slajd 17
 Triplet Triplet su tri uzastopna nukleotida. Slijed tripleta određuje slijed aminokiselina u proteinu! Trojke smještene jedna za drugom, koje određuju strukturu jedne proteinske molekule, predstavljaju GEN.
Triplet Triplet su tri uzastopna nukleotida. Slijed tripleta određuje slijed aminokiselina u proteinu! Trojke smještene jedna za drugom, koje određuju strukturu jedne proteinske molekule, predstavljaju GEN.
slajd 18
 Replikacija je proces samoudvostručavanja molekule DNA koji se temelji na principu komplementarnosti. Značenje replikacije: zbog samodupliciranja DNA dolazi do procesa diobe stanica.
Replikacija je proces samoudvostručavanja molekule DNA koji se temelji na principu komplementarnosti. Značenje replikacije: zbog samodupliciranja DNA dolazi do procesa diobe stanica.
slajd 19
 Između dušikovih baza para A i T stvaraju se 2 vodikove veze, a između G i C - 3, stoga je snaga G-C veze veća od A-T: Komplementarni parovi
Između dušikovih baza para A i T stvaraju se 2 vodikove veze, a između G i C - 3, stoga je snaga G-C veze veća od A-T: Komplementarni parovi
slajd 20

slajd 21

slajd 22
 Važnost nukleinskih kiselina Pohranjivanje, prijenos i nasljeđivanje informacija o strukturi proteinskih molekula. Stabilnost NK je najvažniji uvjet za normalno funkcioniranje stanica i cijelog organizma. Promjena strukture NK - promjena strukture stanica ili fizioloških procesa - promjena vitalne aktivnosti.
Važnost nukleinskih kiselina Pohranjivanje, prijenos i nasljeđivanje informacija o strukturi proteinskih molekula. Stabilnost NK je najvažniji uvjet za normalno funkcioniranje stanica i cijelog organizma. Promjena strukture NK - promjena strukture stanica ili fizioloških procesa - promjena vitalne aktivnosti.
slajd 23
 Korištenje NC Tijekom života, osoba se razboli, uđe u nepovoljne proizvodne ili klimatske uvjete. Posljedica toga je povećanje "kvarova" u dobro funkcionirajućem genetskom aparatu. Do određenog vremena "neuspjesi" se ne manifestiraju prema van i mi ih ne primjećujemo. Jao! S vremenom promjene postaju vidljive. Prije svega, pojavljuju se na koži. Trenutno rezultati istraživanja biomakromolekula izlaze iz zidova laboratorija, počinjući aktivnije pomagati liječnicima i kozmetolozima u njihovom svakodnevnom radu. Davnih 1960-ih. postalo je poznato da izolirani lanci DNA uzrokuju regeneraciju stanica. Ali tek u zadnjim godinama 20. stoljeća postalo je moguće koristiti ovo svojstvo za obnavljanje stanica kože koje stare.
Korištenje NC Tijekom života, osoba se razboli, uđe u nepovoljne proizvodne ili klimatske uvjete. Posljedica toga je povećanje "kvarova" u dobro funkcionirajućem genetskom aparatu. Do određenog vremena "neuspjesi" se ne manifestiraju prema van i mi ih ne primjećujemo. Jao! S vremenom promjene postaju vidljive. Prije svega, pojavljuju se na koži. Trenutno rezultati istraživanja biomakromolekula izlaze iz zidova laboratorija, počinjući aktivnije pomagati liječnicima i kozmetolozima u njihovom svakodnevnom radu. Davnih 1960-ih. postalo je poznato da izolirani lanci DNA uzrokuju regeneraciju stanica. Ali tek u zadnjim godinama 20. stoljeća postalo je moguće koristiti ovo svojstvo za obnavljanje stanica kože koje stare.
slajd 24
 Primjena NC znanosti još je daleko od mogućnosti korištenja egzogenih DNK niti (s izuzetkom virusne DNK) kao predloška za "novu" DNK sintezu izravno u ljudskim, životinjskim ili biljnim stanicama. Činjenica je da je stanica domaćina pouzdano zaštićena od uvođenja strane DNA pomoću specifičnih enzima prisutnih u njoj - nukleaza. Strana DNA će neizbježno proći kroz uništenje ili restrikciju pod djelovanjem nukleaza. DNA će biti prepoznata kao "strana" po odsutnosti u njoj specifičnog obrasca raspodjele metiliranih baza svojstvenih DNA stanice domaćina za svaki organizam. Međutim, što je bliži odnos stanica, to će njihova DNK više formirati hibride. Rezultat ovog istraživanja su razne kozmetičke kreme koje uključuju "čarobne niti" za pomlađivanje kože.
Primjena NC znanosti još je daleko od mogućnosti korištenja egzogenih DNK niti (s izuzetkom virusne DNK) kao predloška za "novu" DNK sintezu izravno u ljudskim, životinjskim ili biljnim stanicama. Činjenica je da je stanica domaćina pouzdano zaštićena od uvođenja strane DNA pomoću specifičnih enzima prisutnih u njoj - nukleaza. Strana DNA će neizbježno proći kroz uništenje ili restrikciju pod djelovanjem nukleaza. DNA će biti prepoznata kao "strana" po odsutnosti u njoj specifičnog obrasca raspodjele metiliranih baza svojstvenih DNA stanice domaćina za svaki organizam. Međutim, što je bliži odnos stanica, to će njihova DNK više formirati hibride. Rezultat ovog istraživanja su razne kozmetičke kreme koje uključuju "čarobne niti" za pomlađivanje kože.
slajd 25
 Učvršćivanje lekcije (kontrolni test) 1. opcija 1. Dvostruki polinukleotidni lanac karakterističan je za molekule: a) DNA b) RNA c) oba prethodna odgovora su točna. 2. Prosječna molekularna težina, koja vrsta nukleinskih kiselina je veća? a) DNA b) RNA c) ovisi o vrsti žive stanice 3. Koje tvari nisu sastavni dio nukleotida? a) pirimidinska ili purinska baza. b) riboza i deoksiriboza c) α - aminokiseline d) fosforna kiselina 4. Nukleotidi DNA ne sadrže ostatke kao baze: a) citozin c) gvanin b) uracil d) adenin e) timin 5. Slijed nukleotida je struktura nukleinske kiseline: a) primarne c) tercijarne b) sekundarne d) kvaternarne 2 opcija 1. Nukleinske kiseline dobile su naziv po latinskoj riječi: a) jezgra c) život b) stanica d) prva 2. Polimerni lanac, koji od nukleinskih kiseline je niz nukleotida ? a) DNA b) RNA c) obje vrste nukleinskih kiselina 3. Sekundarna struktura u obliku dvostruke spirale karakteristična je za molekule: a) DNA c) RNA b) proteini d) sve nukleinske kiseline 4. Purinska baza nije: a) adenin c) gvanin b) timin d) svi su 5. Molekula nukleotida ne sadrži: a) ostatak monosaharida c) ostatak dušične baze b) ostatak aminokiseline d) ostatak fosforne kiseline
Učvršćivanje lekcije (kontrolni test) 1. opcija 1. Dvostruki polinukleotidni lanac karakterističan je za molekule: a) DNA b) RNA c) oba prethodna odgovora su točna. 2. Prosječna molekularna težina, koja vrsta nukleinskih kiselina je veća? a) DNA b) RNA c) ovisi o vrsti žive stanice 3. Koje tvari nisu sastavni dio nukleotida? a) pirimidinska ili purinska baza. b) riboza i deoksiriboza c) α - aminokiseline d) fosforna kiselina 4. Nukleotidi DNA ne sadrže ostatke kao baze: a) citozin c) gvanin b) uracil d) adenin e) timin 5. Slijed nukleotida je struktura nukleinske kiseline: a) primarne c) tercijarne b) sekundarne d) kvaternarne 2 opcija 1. Nukleinske kiseline dobile su naziv po latinskoj riječi: a) jezgra c) život b) stanica d) prva 2. Polimerni lanac, koji od nukleinskih kiseline je niz nukleotida ? a) DNA b) RNA c) obje vrste nukleinskih kiselina 3. Sekundarna struktura u obliku dvostruke spirale karakteristična je za molekule: a) DNA c) RNA b) proteini d) sve nukleinske kiseline 4. Purinska baza nije: a) adenin c) gvanin b) timin d) svi su 5. Molekula nukleotida ne sadrži: a) ostatak monosaharida c) ostatak dušične baze b) ostatak aminokiseline d) ostatak fosforne kiseline