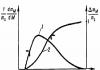
Исследования зависимости давления газа от температуры при условии неизменного объема определенной массы газа впервые были произведены в 1787 г. Жаком Александром Сезаром Шарлем (1746 – 1823). Можно воспроизвести эти опыты в упрощенном виде, нагревая газ в большой колбе, соединенной с ртутным манометром М в виде узкой изогнутой трубки (рис. 6).
Пренебрежем ничтожным увеличением объема колбы при нагревании и незначительным изменением объема при смещении ртути в узкой манометрической трубке. Таким образом, можно считать объем газа неизменным. Подогревая воду в сосуде, окружающем колбу, будем отмечать температуру газа по термометру Т , а соответствующее давление – по манометру М . Наполнив сосуд тающим льдом, измерим давление p 0 , соответствующее температуре 0 °C.
Опыты подобного рода показали следующее.
1. Приращение давления некоторой массы составляет определенную часть α того давления, которая имела данная масса газа при температуре 0 °C. Если давление при 0 °C обозначить через p 0 , то приращение давления газа при нагревании на 1 °C есть p 0 +αp 0 .
При нагревании на τ приращение давления будет в τ раз больше, т.е. приращение давления пропорционально приращению температуры .
2. Величина α, показывающая, на какую часть давления при 0 °C увеличивается давление газа при нагревании на 1 °C, имеет одно и то же значение (точнее, почти одно и тоже) для всех газов, а именно 1/273 °C -1 . Величину α называют температурным коэффициентом давления. Таким образом, температурный коэффициент давления для всех газов имеет одно и то же значение, равное 1/273 °C -1 .
Давление некоторой массы газа при нагревании на 1 °C при неизменном объеме увеличивается на 1/273 часть давления, которое эта масса газа имела при 0 °C (закон Шарля ).
Следует, однако, иметь в виду, что температурным коэффициентом давления газа, полученный при измерении температуры по ртутному манометру, не в точности одинаков для разных температур: закон Шарля выполняется только приближенно, хотя и с очень большой степенью точности.
Формула, выражающая закон Шарля.
Закон Шарля позволяет рассчитывать давление газа при любой температуре, если известно его давление при температуре
0 °C. Пусть давление данной массы газа при 0 °C в данном объеме есть p
0 , а давление того же газа при температуре t
есть p
. Приращение температуры есть t
, следовательно, приращение давления равно αp
0 t
и искомое давление
Этой формулой можно пользоваться также и в том случае, если газ охлажден ниже 0 °C; при этом t будет иметь отрицательные значения. При очень низких температурах, когда газ приближается к состоянию сжижения, а также в случае сильно сжатых газов закон Шарля неприменим и формула (2) перестает быть годной.
Закон Шарля с точки зрения молекулярной теории. Что происходит в микромире молекул, когда температура газа меняется, например, когда температура газа повышается и давление его увеличивается? С точки зрения молекулярной теории возможны две причины увеличения давления данного газа: во-первых, могло увеличиться число ударов молекул за единицу времени на единицу площади, во-вторых, мог увеличиться импульс, передаваемый при ударе в стенку одной молекулой. И та, и другая причина требуют увеличения скорости молекул (напоминаем, что объем данной массы газа остается неизменным). Отсюда становится ясным, что повышение температуры газа (в макромире) есть увеличение средней скорости беспорядочного движения молекул (в микромире).
Некоторые типы электрических ламп накаливания наполняют смесью азота и аргона. При работе лампы газ в ней нагревается примерно до 100 °C. Какое должно быть давление смеси газов при 20 °C, если желательно, чтобы при работе лампы давление газа в ней не превышало атмосферного? (ответ: 0,78 кгс/см 2)
На манометрах ставится красная черта, указывающая предел, свыше которого увеличение газа опасно. При температуре 0 °C манометр показывает, что избыток давления газа над давлением наружного воздуха равен 120 кгс/см 2 . Будет ли достигнута красная черта при повышении температуры до 50 °C, если красная черта стоит на 135 кгс/см 2 ? Давление наружного воздуха принять равным 1 кгс/см 2 (ответ: стрелка манометра перейдет за красную черту)
Связь между давлением, температурой, объемом и количеством молей газа ("массой" газа). Универсальная (молярная) газовая постоянная R. Уравнение Клайперона-Менделеева = уравнение состояния идеального газа.
|
Ограничения практической применимости:
Внутри диапазона точность уравнения превосходит точность обычных современных инженерных средств измерения. Для инженера важно понимать, что для всех газов возможна существенная диссоциация или разложение при повышении температуры. |
|
|
|
Давайте решим парочку задач относительно газовых объемных и массовых расходов в предположении, что состав газа не изменяется (газ не диссоциирует) - что верно для большинства газов в указанных выше .
Данная задача актуальна в основном, но не только, для применений и устройств, в которых напрямую измеряется объем газа.
V 1 и V 2 , при температурах, соответственно, T 1 и T 2 и, пусть T 1 < T 2 . Тогда мы знаем, что:
Естественно, V 1 < V 2
- показатели объемного счетчика газа тем "весомее", чем ниже температура
- выгодно поставлять "теплый" газ
- выгодно покупать "холодный" газ
Как с этим бороться? Необходима хотя бы простая температурная компенсация, т.е в считающее устройство должна подаваться информация с дополнительного датчика температуры.
Данная задача актуальна в основном, но не только, для применений и устройств, в которых напрямую измеряется скорость газа.
Пусть счетчик () в точке доставки дает объемные накопленные расходы V 1 и V 2 , при давлениях, соответственно, P 1 и P 2 и, пусть P 1 < P 2 . Тогда мы знаем, что:
Естественно, V 1 >V 2 для одинаковых количеств газа при данных условиях. Попробуем сформулировать несколько важных на практике выводов для данного случая:
- показатели объемного счетчика газа тем "весомее", чем выше давление
- выгодно поставлять газ низкого давления
- выгодно покупать газ высокого давления
Как с этим бороться? Необходима хотя бы простая компенсация по давлению, т.е в считающее устройство должна подаваться информация с дополнительного датчика давления.
В заключение, хотелось бы отметить, что, теоретически, каждый газовый счетчик должен иметь и температурную компенсацию и компенсацию по давлению. Практически же......
Уравнение состояния идеального газа определяет связь температуры, объема и давления тел.
- Позволяет определить одну извеличин, характеризующих состояние газа, по двум другим (используется в термометрах);
- Определить, как протекают процессы при определенных внешних условиях;
- Определить, как меняется состояние системы, если она совершает работу или получает тепло от внешних тел.
Уравнение Менделеева-Клапейрона (уравнение состояния идеального газа)
- универсальная газовая постоянная , R = kN A
Уравнение Клапейрона (объединенный газовый закон)
Частными случаями уравнения являются газовые законы, описывающие изопроцессы в идеальных газах, т.е. процессы, при которых один из макропараметров (T, P, V) в закрытой изолированной системе постоянный.
Количественные зависимости между двумя параметрами газа одной и той же массы при неизменном значении третьего параметра называют газовыми законами.
Газовые законы
Закон Бойля - Мариотта
Первый газовый закон был открыт английским ученым Р. Бойлем (1627-1691) в 1660 г. Работа Бойля называлась «Новые эксперименты, касающиеся воздушной пружины». И действительно, газ ведет себя подобно сжатой пружине, в этом можно убедиться, сжимая воздух в обычном велосипедном насосе.
Бойль изучал изменение давления газа в зависимости от объема при постоянной температуре. Процесс изменения состояния термодинамической системы при постоянной температуре называют изотермическим (от греческих слов isos - равный, therme - тепло).
Независимо от Бойля несколько позднее французский ученый Э. Мариотт (1620-1684) пришел к тем же выводам. Поэтому найденный закон получил название закона Бойля-Мариотта.
Произведение давления газа данной массы на его объем постоянно, если температура не меняется
pV = const
Закон Гей-Люссака
Сообщение об открытии еще одного газового закона было опубликовано лишь в 1802 г., спустя почти 150 лет после открытия закона Бойля-Мариотта. Закон, определяющий зависимость объема газа от температуры при постоянном давлении (и неизменной массе), был установлен французским ученым Гей-Люссаком (1778- 1850).
Относительное изменение объема газа данной массы при постоянном давлении прямо пропорционально изменению температуры
V = V 0 αT
Закон Шарля
Зависимость давления газа от температуры при постоянном объеме экспериментально установил французский физик Ж. Шарль (1746-1823) в 1787 г.
Ж. Шарль в 1787 г., т. е. раньше, чем Гей-Люссак, установил и зависимость объема от температуры при постоянном давлении, но он своевременно не опубликовал своих работ.
Давление данной массы газа при постоянном объеме прямо пропорционально абсолютной температуре.
p = p 0 γT
| Название | Формулировка | Графики |
|
Закон Бойля-Мариотта – изотермическ ий процесс |
Для данной массы газа произведение давления на объем постоянно, если температура не меняется |
   |
|
Закон Гей-Люссака – изобарный процесс |
Связь между давлением, температурой, объемом и количеством молей газа ("массой" газа). Универсальная (молярная) газовая постоянная R. Уравнение Клайперона-Менделеева = уравнение состояния идеального газа.
|
Ограничения практической применимости:
Внутри диапазона точность уравнения превосходит точность обычных современных инженерных средств измерения. Для инженера важно понимать, что для всех газов возможна существенная диссоциация или разложение при повышении температуры. |
|
|
|
Давайте решим парочку задач относительно газовых объемных и массовых расходов в предположении, что состав газа не изменяется (газ не диссоциирует) - что верно для большинства газов в указанных выше .
Данная задача актуальна в основном, но не только, для применений и устройств, в которых напрямую измеряется объем газа.
V 1 и V 2 , при температурах, соответственно, T 1 и T 2 и, пусть T 1 < T 2 . Тогда мы знаем, что:
Естественно, V 1 < V 2
- показатели объемного счетчика газа тем "весомее", чем ниже температура
- выгодно поставлять "теплый" газ
- выгодно покупать "холодный" газ
Как с этим бороться? Необходима хотя бы простая температурная компенсация, т.е в считающее устройство должна подаваться информация с дополнительного датчика температуры.
Данная задача актуальна в основном, но не только, для применений и устройств, в которых напрямую измеряется скорость газа.
Пусть счетчик () в точке доставки дает объемные накопленные расходы V 1 и V 2 , при давлениях, соответственно, P 1 и P 2 и, пусть P 1 < P 2 . Тогда мы знаем, что:
Естественно, V 1 >V 2 для одинаковых количеств газа при данных условиях. Попробуем сформулировать несколько важных на практике выводов для данного случая:
- показатели объемного счетчика газа тем "весомее", чем выше давление
- выгодно поставлять газ низкого давления
- выгодно покупать газ высокого давления
Как с этим бороться? Необходима хотя бы простая компенсация по давлению, т.е в считающее устройство должна подаваться информация с дополнительного датчика давления.
В заключение, хотелось бы отметить, что, теоретически, каждый газовый счетчик должен иметь и температурную компенсацию и компенсацию по давлению. Практически же......
Убедимся в том, что молекулы газа действительно расположены достаточно далеко друг от друга, и поэтому газы хорошо сжимаемы.Возьмем шприц и расположим его поршень приблизительно посередине цилиндра. Отверстие шприца соединим с трубкой, второй конец которой наглухо закрыт. Таким образом, некоторая порция воздуха будет заключена в цилиндре шприца под поршнем и в трубке.В цилиндре под поршнем заключено некоторое количество воздуха. Теперь поставим на подвижный поршень шприца груз. Легко заметить, что поршень немного опустится. Это означает, что объем воздуха уменьшился Другими словами, газы легко сжимаются. Таким образом, между молекулами газа имеются достаточно большие промежутки. Помещение груза на поршень вызывает уменьшение объема газа. С другой стороны, после установки груза поршень, немного опустившись, останавливается в новом положении равновесия. Это означает, что сила давления воздуха на поршень увеличивается и снова уравновешивает возросший вес поршня с грузом. А поскольку площадь поршня при этом остается неизменной, мы приходим к важному заключению.
При уменьшении объема газа его давление увеличивается.
Будем помнить при этом, что масса газа и его температура в ходе опыта оставались неизменными . Объяснить зависимость давления от объема можно следующим образом. При увеличении объема газа расстояние между его молекулами увеличивается. Каждой молекуле теперь нужно пройти большее расстояние от одного удара со стенкой сосуда до другого. Средняя скорость движения молекул остается неизменной.Следовательно, молекулы газа реже ударяются о стенки сосуда, а это приводит к уменьшению давления газа. И, наоборот, при уменьшении объема газа его молекулы чаще ударяются о стенки сосуда, и давление газа увеличивается. При уменьшении объема газа расстояние между его молекулами уменьшается
Зависимость давления газа от температуры
В предыдущих опытах температура газа оставалась неизменной, и мы изучали изменение давления вследствие изменения объема газа. Теперь рассмотрим случай, когда объем газа остается постоянным, а температура газа изменяется. Масса при этом также остается неизменной. Создать такие условия можно, поместив некоторое количество газа в цилиндр с поршнем и закрепив поршень
Изменение температуры данной массы газа при неизменном объеме
Чем выше температура, тем быстрее движутся молекулы газа .
Следовательно,
Во-первых, чаще происходят удары молекул о стенки сосуда;
Во-вторых, средняя сила удара каждой молекулы о стенку становится больше. Это приводит нас к еще одному важному заключению. При увеличении температуры газа его давление увеличивается. Будем помнить, что данное утверждение справедливо, если масса и объем газа в ходе изменения его температуры остаются неизменными.
Хранение и транспортировка газов.
Зависимость давления газа от объема и температуры часто используется в технике и в быту. Если требуется перевезти значительное количество газа из одного места в другое, или когда газы необходимо длительно хранить, их помещают в специальные прочные металлические сосуды. Эти сосуды выдерживают высокие давления, поэтому с помощью специальных насосов туда можно закачать значительные массы газа, которые в обычных условиях занимали бы в сотни раз больший объем. Поскольку давление газов в баллонах даже при комнатной температуре очень велико, их ни в коем случае нельзя нагревать или любым способом пытаться сделать в них отверстие даже после использования.
Газовые законы физики.
Физика реального мира в расчетах часто сводится к несколько упрощенным моделям. Наиболее применим такой подход к описанию поведения газов. Правила, установленные экспериментальным путем, были сведены различными исследователями в газовые законы физики и послужили появлению понятия «изопроцесс». Это такое прохождение эксперимента, при котором один параметр сохраняет постоянное значение. Газовые законы физики оперируют основными параметрами газа, точнее, его физического состояния. Температурой, занимаемым объемом и давлением. Все процессы, которые относятся к изменению одного или нескольких параметров и называются термодинамическими. Понятие изостатического процесса сводится к утверждению, что во время любого изменения состояния один из параметров остается неизменным. Это поведение так называемого «идеального газа», которое, с некоторыми оговорками, может быть применено к реальному веществу. Как отмечено выше, в реальности все несколько сложнее. Однако, с высокой достоверностью поведение газа при неизменной температуре характеризуется с помощью закона Бойля-Мариотта, который гласит:
Произведение объема на давление газа - величина постоянная. Это утверждение считается верным в том случае, когда температура не изменяется.
Этот процесс носит название «изотермический». При этом меняются два из трех исследуемых параметров. Физически все выглядит просто. Сожмите надутый шарик. Температуру можно считать неизменной. А в результате внутри шара повысится давление при уменьшении объема. Величина произведения двух параметров останется неизменной. Зная исходное значение хотя бы одного из них, можно легко узнать показатели второго. Еще одно правило в списке «газовые законы физики» - изменение объема газа и его температуры при одинаковом давлении. Это называется «изобарный процесс» и описывается с помощью закона Гей-Люсака. Соотношение объема и температуры газа неизменно. Это верно при условии постоянного значения давления в данной массе вещества. Физически тоже все просто. Если хоть раз заряжали газовую зажигалку или пользовались углекислотным огнетушителем, видели действие этого закона «вживую». Газ, выходящий из баллончика или раструба огнетушителя, быстро расширяется. Его температура резко падает. Можно обморозить кожу рук. В случае с огнетушителем - образуются целые хлопья углекислотного снега, когда газ под воздействием низкой температуры быстро переходит в твердое состояние из газообразного. Благодаря закону Гей-Люсака, можно легко узнать температуру газа, зная его объем в любой момент времени. Газовые законы физики описывают и поведение при условии неизменного занимаемого объема. Такой процесс называется изохорным и описывается законом Шарля, который гласит: При неизменном занимаемом объеме, отношение давления к температуре газа остается неизменным в любой момент времени. В реальности все знают правило: нельзя нагревать баллончики от освежителей воздуха и прочие сосуды, содержащие газ под давлением. Дело кончается взрывом. Происходит именно то, что описывает закон Шарля. Растет температура. Одновременно растет давление, так как объем не меняется. Происходит разрушение баллона в момент, когда показатели превышают допустимые. Так что, зная занимаемый объем и один из параметров, можно легко установить значение второго. Хотя газовые законы физики описывают поведение некой идеальной модели, их можно легко применять для предсказания поведения газа в реальных системах. Особенно в быту, изопроцессы могут легко объяснить, как работает холодильник, почему из баллончика освежителя вылетает холодная струя воздуха, из-за чего лопается камера или шарик, как работает разбрызгиватель и так далее.
Основы МКТ.
Молекулярно-кинетическая теория вещества - способ объяснения тепловых явлений , который связывает протекание тепловых явлений и процессов с особенностями внутреннего строения вещества и изучает причины, которые обусловливают тепловое движение. Эта теория получила признание лишь в XX в., хотя исходит из древнегреческого атомного учения о строении вещества.
объясняет тепловые явления особенностями движения и взаимодействия микрочастиц вещества
Основывается на законах классической механики И. Ньютона, которые позволяют вывести уравнение движения микрочастиц. Тем не менее в связи с огромным их количеством (в 1 см 3 вещества находится около 10 23 молекул) невозможно ежесекундно с помощью законов классической механики однозначно описать движение каждой молекулы или атома. Поэтому для построения современной теории теплоты используют методы математической статистики, которые объясняют течение тепловых явлений на основании закономерностей поведения значительного количества микрочастиц.
Молекулярно-кинетическая теория построена на основании обобщенных уравнений движения огромного количества молекул.
Молекулярно-кинетическая теория объясняет тепловые явления с позиций представлений о внутреннем строении вещества, то есть выясняет их природу. Это более глубокая, хотя и более сложная теория, которая объясняет сущность тепловых явлений и обусловливает законы термодинамики.
Оба существующих подхода - термодинамический подход и молекулярно-кинетическая теория - научно доказаны и взаимно дополняют друг друга, а не противоречат друг другу. В связи с этим изучение тепловых явлений и процессов обычно рассматривается с позиций или молекулярной физики, или термодинамики, в зависимости от того, как проще изложить материал.
Термодинамический и молекулярно-кинетический подходы взаимно дополняют друг друга при объяснении тепловых явлений и процессов.