К таким факторам относят: величину U0, ММ полимера, густоту пространственной сетки, размер заместителей и температуру.
Потенциальный барьер вращения (U0). Величина U0 зависит от внутри- и межмолекулярных взаимодействий. Рассмотрим факторы, влияющие на U0 и гибкость цепей у карбоцепных полимеров.
У карбоцепных полимеров наименее полярными являются предельные углеводороды. У них внутри- и межмолекулярные взаимодействия невелики, а также малы значения U0 и ΔU, следовательно полимеры обладают большой кинетической и термодинамической гибкостью. Примеры: ПЭ, ПП, ПИБ.
Особенно низки значения U0 у полимеров, в цепи которых рядом с ординарной имеется двойная связь.
–СН2–СН=СН–СН2– Полибутадиен
Введение в макромолекулы заместителей, содержащих полярные группы приводит к внутри- и межмолекулярным взаимодействиям. При этом существенно влияют степень полярности групп и симметричность их расположения:
Наиболее полярные группы –СN, –NO2 (μ=3,4 D)
Менее полярные группы –Cl, –OH (μ=1,8-1,9 D)
При введении полярных групп возможны три случая по влиянию на гибкость:
1. Полярные группы близко расположены и возможны между ними сильные взаимодействия. Переход такими полимерами из одного пространственного положения в другое требует преодоления больших U0, поэтому цепи таких полимеров наименее гибкие.
2. Полярные группы расположены в цепи редко и взаимодействия между ними не проявляются. Значения U0 и ΔU невелики и полимеры имеют большую кинетическую и термодинамическую гибкость.
3.Полярные группы расположены так, что электрические поля взаимно компенсируются. При этом суммарный дипольный момент макромолекулы равен нулю. Поэтому низки значения U0 и ΔU и полимеры имеют большую кинетическую и термодинамическую гибкость.
Политетрафторэтилен –СF2–СF2–
Гетероцепные полимеры
У гетероцепных полимеров вращение возможно вокруг связей С–О, С–N, Si–O, C–C. Значения U0 для этих связей невелики и цепи обладают достаточной кинетической гибкостью. Примеры: полиэфиры, полиамиды, полиуретаны, силоксановые каучуки.
Однако гибкость гетероцепных полимеров может ограничиваться межмолекулярными взаимодействиями за счёт образования Н-связей (например, у целлюлозы, полиамидов). Целлюлоза является одним из жесткоцепных полимеров. У неё содержится большое количество полярных групп (–OH) и поэтому для целлюлозы характерны внутри- и межмолекулярные взаимодействия и высокие значения U0 и малая гибкость.
Молекулярная масса полимера. Увеличение ММ полимера повышает свернутость цепи и поэтому длинные макромолекулы обладают большей кинетической гибкостью по сравнению с короткими макромолекулами. По мере увеличения ММ возрастает число конформаций, которое может принимать макромолекула и гибкость цепей увеличивается.
Густота пространственной сетки. Чем больше химических связей между макромолекулами, тем меньше гибкость цепей, т.е. с увеличением густоты пространственной сетки гибкость уменьшается. Примером является снижение гибкости цепей с увеличением числа сшивок в ряду резол<резитол<резит.
Влияние размера и количества заместителей. Увеличение числа полярных и больших по размеру заместителей снижает подвижность звеньев макромолекулы и уменьшает кинетическую гибкость. Примером является снижение гибкости макромолекул сополимера бутадиена и стирола при увеличении содержания громоздких фенильных заместителей в цепи. Если при одном атоме углерода в основной цепи полимера имеются два заместителя (например, ОСН3 и СН3 в звеньях ПММА), то макромолекула становится кинетически жесткой.
Температура. С повышением температуры возрастает кинетическая энергия макромолекулы. До тех пор, пока величина кинетической энергии меньше U0, цепи совершают крутильные колебания. Когда кинетическая энергия макромолекулы становится равной или превышает величину U0 звенья начинают вращаться. С повышением температуры величина U0 мало изменяется, а скорость поворота звеньев увеличивается и кинетическая гибкость возрастает.
Химические превращения макромолекул используются для получения новых полимеров и модификации свойств готовых полимеров. Такие превращения могут осуществляться как направленно, так и самопроизвольно в процессе синтеза, переработки и эксплуатации полимеров под действием света, кислорода воздуха, тепла и механических воздействий. Основными разновидностями химических превращений полимеров являются:
1) Реакции, протекающие без изменения степени полимеризации (внутримолекулярные и полимераналогичные превращения),
2) Реакции, приводящие к увеличению степени полимеризации (сшивание и отверждение полимеров, получение блок- и привитых сополимеров),
3) Реакции, приводящие у уменьшению степени полимеризации (деструкция полимеров).
Особенности химических реакций полимеров
Химические реакции полимеров не отличаются от классических органических реакций, однако вследствие больших размеров макромолекул и сложности их строения реакции полимеров имеют специфические особенности.
Основными отличиями реакций полимеров от реакций низкомолекулярных соединений являются:
Для полимеров возможны реакции, не присущие низкомолекулярным соединениям, например, деполимеризация. Деполимеризация – это последовательное отщепление от цепи звеньев мономера.
В отличие от реакций низкомолекулярных соединений, когда конечные и промежуточные продукты реакций можно от делить от исходных соединений, в случае реакций полимеров конечные и промежуточные продукты входят в состав одной и той же макромолекулы и их невозможно разделить. Например, при этерификации низкомолекулярного спирта на каждой стадии реакции в системе находятся спирт, кислота, сложный эфир и вода, которые могут быть разделены. При этерификации поливинилового спирта промежуточными продуктами реакции являются сополимеры, содержащие гидроксильные и сложноэфирные группы, которые невозможно разделить:
Реакционная способность функциональных групп макромолекул отличается от реакционной способности низкомолекулярных соединений. Причиной является цепная природа полимера, когда “принцип равной реакционной способности” Флори не соблюдается. Устарело представление, что реакционная способность функциональных групп не должна зависить от длины полимерной цепи.
Основными особенностями в химическом поведении полимеров по сравнению с низкомолекулярными аналогами являются конфигурационный, конформационный, концентрационный.
Надмолекулярный, электростатический эффекты и “эффект соседа”.
Конфигурационный эффект - это различие в окружении функциональных групп полимера в начале и в конце реакции, которое отражается на направлении и завершенности реакции, на кинетике и механизме реакции.
На реакционную способность полимеров при химических превращениях существенное влияние оказывает стереоизомерия цепи. Например, цис -изомер – натуральный каучук отличается при химических превращениях от транс -изомера – гуттаперчи. Расположение функциональных групп по длине цепи также влияет на их химические свойства. Например, макромолекулы ПВС “нормального” строения (соединение звеньев по типу “голова к хвосту”) не подвергаются деструкции под действием кислорода и иодной кислоты (HIO4), а макромолекулы ПВС аномального строения (соединение звеньев по типу “голова к голове”) легко деструктируются.
Другой пример, при расположении звеньев в цепи ПВХ по типу “голова к хвосту” дегидрохлорирование и термический распад макромолекул протекает медленно, а при расположении звеньев в цепи по типу “голова к голове” реакция протекает быстро.
ПВХ Полихлоропрен
“Эффект соседа” . В полимерах изменение реакционной способности функциональных групп или звеньев под влиянием уже прореагировавшей группы, расположенной по соседству в данной называется “эффектом соседа”. Влияние “соседей” вызывает изменение скорости и механизма реакций в полимерах. При этом скорость реакции может повышаться в 103–104 раз. Наряду с ускоряющим действием “соседи” могут оказывать и ингибирующее влияние на скорость реакции.
3. Молекулярная масса полимеров и молекулярно-массовое распределение (ММР). Полидисперсность полимеров. Среднечисловая, средневязкостная и среднемассовая молекулярная масса полимеров. Способы определения молекулярных масс полимеров.
Большинство синтетических полимеров состоит из макромолекул различной длины, т.е. являются полидисперсными вследствие статистического (случайного) характера элементарных реакций синтеза и возможности деструкции макромолекул. Биополимеры обычно однородны по молекулярной массе (ММ), однако при выделении полимеров некоторые связи разрушаются и биополимеры становятся полидисперсными.
Вследствие полидисперсности полимеры характеризуют средними ММ и в зависимости от типа усреднения различают среднечисловую и среднемассовую ММ. Существуют и другие типы усреднения, так при исследовании гидродинамических свойств полимеров определяют среднегидродинамические ММ. Такие ММ определяют при измерении вязкости (средневязкост ная –M η), константы седиментации (среднеседиментационна я – M S) или коэффициента диффузии (среднедиффузионная –M D).
Среднечисловая молекулярная масса определяется соотношением:
Здесь N – число макромолекул, xi – числовая доля макромолекул с молекулярной массой Mi. xi= Ni / ΣN i .
Экспериментально n M измеряют методами, в основе которых лежат коллигативные свойства растворов (зависящие от числа частиц). К таким методам относят осмометрию, криоскопию, эбулиоскопию и анализ концевых групп.
Среднемассовая молекулярная масса определяется соотношением:
Здесь N – число макромолекул, ωi – массовая доля макромолекул с молекулярной массой Mi. ωi = Ni Mi / Σ N i Mi . Экспериментально M ω определяют методом светорассеяния. Величина M ω > n M для полидисперсного образца и M ω=Mn для монодисперсного образца. Значения M ω более чувствительны к наличию в образце высокомолекулярных фракций, а n M – к наличию низкомолекулярных фракций.
Отношение M ω/ n M =К D называется показателем полидисперсности. Если образец монодисперсен, то К D=1 (редкий случай). Для большинства синтетических и природных полимеров К D>1, т.е. полимеры полидисперсны, причём К D может изменяться в широких пределах (от 2 до 20). Значения показателя полидисперсности К D связаны с механизмом образования полимера. Так, К D=1,5 для продукта радикальной полимеризации при обрыве цепи рекомбинацией и К D=2 – при обрыве цепи диспропорционированием. Для полимеров, полученных поликонденсацией, К D=1 + Х, где Х – конверсия. При Х→1 (100%) К D=2.
Для характеристики полидисперсности полимеров, кроме показателя полидисперсности, используются кривые молекулярно-массового распределения (ММР). Различают интегральные и дифференциальные функции ММР (рис. 1), которые могут быть числовыми и массовыми. Интегральная кривая ММР – это зависимость между ММ и интегральной массовой (или числовой) долей фракций полимера.
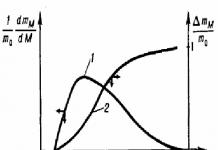
Дифференциальная кривая ММР представляет собой зависимость ММ от массовой [молекулярно-массовое распределение (ММР) (рис.2, кривая 2)] или числовой доли фракции [молекулярно-числовое распределение (МЧР) (рис. 2, кривая 1)]. КривыеМЧР и ММР не совпадают, т.к на числовое распределение большое влияние оказывают низкомолекулярные фракции, а на массовое распределение влияют высокомолекулярные фракции.
Абсцисса центра тяжести площади, ограниченной кривой ММР, равна M ω , а абсцисса центра тяжести площади, ограниченной кривой МЧР, равна n M (см. рис.2). Кривые распределения могут иметь один (унимодальные), два (бимодальные) или несколько максимумов (полимодальные).
При одинаковой средней ММ полимеры могут иметь различное ММР – узкое (на рис. 3, кривая 2) и широкое (рис. 3, кривая 1).

Рис. 1. Кривые интегрального (2) и дифференциального (1) массового ММР полимера.
Здесь Δ m / m0 – относительная интегральная доля фракций, а (1/ m0)(d m/d M) – массовая доля фракций.

Рис. 2. Дифференциальные кривые МЧР (1) и ММР(2).

Рис. 3. Кривые ММР с различной полидисперсностью и одинаковым значением средней ММ.
Фракционирование полимеров
Фракционирование позволяет разделять образцы полимеров на фракции с различными ММ и используется для построения кривых ММР. Различают два типа фракционирования: препаративное и аналитическое . При препаративном фракционировании выделяют отдельные фракции и изучают их свойства. При аналитическом фракционировании кривую распределения получают без выделения отдельных фракций. К аналитическим методам фракционирования относят ультрацентрифугирование, турбодиметрическое титрование, гель-проникающую хроматографию.
К препаративным методам фракционирования относятся фракционное растворение и фракционное осаждение . Эти методы основаны на зависимости растворимости полимера от ММ – с увеличением ММ растворимость полимера уменьшается. Метод фракционного осаждения заключается в последовательном осаждении из раствора полимера фракций, ММ которых убывает. Осаждение фракций вызывают различными способами:
Добавлением осадителя к раствору полимера,
Испарением растворителя из раствора полимера,
Изменением температуры раствора, которое ухудшает качество растворителя.
Метод фракционного растворения заключается в последовательном экстрагировании полимера рядом жидкостей с возрастающей растворяющей способностью. При этом выделяемые фракции имеют последовательно возрастающую ММ.
Построение кривых распределения по ММ
В результате фракционирования выделяют ряд фракций. Для каждой фракции определяют массу и находят ММ. Экспериментальные данные вносят в таблицу.
Затем определяют массовую долю каждой фракции ωi и далее определяют интегральную массовую долю фракций суммированием всех долей фракций, начиная с наименьшей по ММ фракции. Расчётные данные вносят в таблицу.
По данным таблицы строят интегральную кривую ММР в координатах Wi=f (ММ) и дифференциальную кривую ММР в координатах dWi /dMi=f (ММ).
4. Изомерия высокомолекулярных соединений. Особенности изомерии полимерных материалов, понятие ближнего и дальнего порядка. Конформационная и конфигурационная изомерия элементарного звена.
Локальная изомерия
Этот вид изомерии характерен для виниловых, винилиденовых и диеновых полимеров. Так у молекулы винилового мономера
Заместители при атомах С (1) (голова) и (2) (хвост) различаются и, следовательно, возможны два типа присоединения

Присоединение по типу “голова-голова” происходят значительно реже, чем присоединения “голова-хвост” прежде всего из-за возникающих стерических затруднений. Так, например, в поливинилиденфториде (-СH 2 -CF 2 -) n доля звеньев присоединённых по типу “голова-голова” составляет всего 5-6%.
Образование молекул полиизопрена может происходить путём присоединения молекул мономеров в положениях 1,4; 1,2; 3,4. При этом будут образовываться различающиеся по конфигурации изомеры:

(У полибутадиена вследствие симметричного строения молекулы мономера возможно только присоединение 1,4 и 1,2). В зависимости от природы катализатора и условий полимеризации доля различных конфигураций в полимерных цепях может изменяться в широких пределах. У полиизопрена наряду с изомерией, обусловленной способом присоединения по двойным связям существует также изомерия присоединения по типу “голова-хвост” и “голова-голова”.
20.09.11 11:10
Отклонения от равновесного состояния на коротких участках цепи вызывают на длинных участках проявление такого свойства полимера, как гибкость.
Количественными характеристиками гибкости макромолекулы могут служить персистентная длина, статистический сегмент, среднеквадратичное расстояние между концами цепи, средний квадрат радиуса инерции макромолекулы.
Среднеквадратичное расстояние между концами цепи . Конформация полимерного клубка постоянно меняется, отклоняется от равновесной. Расстояние между концами цепи при этом меняется. Чтобы узнать, какое расстояние между концами цепи наиболее часто реализуется, надо взять все значения, полученные в ходе измерений, и поделить на число измерений – т.е. найти среднее значение (рис. 8):
Рис. 8 Расстояние между концами цепи (слева) и радиус инерции (справа) в представлении свободно-сочлененной модели цепи
Зная длину жесткого сегмента
l N
и количество таких сегментов в цепи
N
, можно рассчитать
Вращение жестких участков на шарнирах свободно. Для такой модели
Модель с фиксированными валентными углами b . Отличается от предыдущей модели тем, что между двумя соседними сегментами фиксируется угол. Вращение вокруг осей остается свободным. В таком случае
Поворотно-изомерная модель . В этой модели, кроме фиксированных валентных углов, появляется заторможенное внутреннее вращение,определяемое величиной торсионного угла
Для идеального клубка, зная
Средние размеры макромолекулы также можно выразить через контурную длину цепи L . Контурная длина цепи определяется числом мономерных звеньев или СПЗ, образующих макромолекулу. Если поделить цепь на жесткие участки равной длины, т о
Отсюда можно записать, используя свободно-сочлененную модель
Такая модель справедлива для оценки термодинамической гибкости макромолекул гибкоцепных полимеров (l N £ 100 Å или 10 нм).
Из выражений (1), (2) можно найти величину наименьшего жесткого участка цепи (сегмента Куна ) :
Исходя из выражения (3), для объема клубка можно записать
Гауссово распределение расстояний между концами цепи
Типичная конформация полимерного клубка имеет очевидное сходство с траекторией движения броуновской частицы (рис. 9б).
Вектор r , определяющий расстояние между концами цепи, сильно флуктуирует из-за теплового движения. Рассмотрим распределение вероятности вектора r между концами цепи из N сегментов для свободно-сочлененной модели идеальной цепи. Так как каждый сегмент дает независимый вклад в r , то, по аналогии с траекторией броуновской частицы, для величины r будет справедливо гауссово распределение (поэтому идеальный клубок часто называют гауссовым клубком)
Гибкость макромолекул – одна из важнейших характеристик полимера, определяющая его основные макроскопические свойства. Гибкость макромолекул − это способность полимерных цепей изменять свою конформацию в результате внутримолекулярного теплового движения звеньев (термодинамическая гибкость ) или же под действием внешних механических сил (кинетическая гибкость ). Гибкость макромолекул обусловлена тем, что мономерные звенья цепи при тепловом движении или при внешних силовых воздействиях вращаются вокруг одинарных (s-) связей.
Представление о внутреннем вращении макромолекул полимеров впервые было введено Куном, Марком и Гутом. При вращении звеньев макромолекула изменяет свою форму. Формы макромолекулы, переходящие друг в друга без разрыва химических связей, называют конформациями . Известно много типов конформаций макромолекул: конформация клубка, конформация вытянутой жёсткой палочки, конформация спирали, конформация глобулы (самая компактная), складчатая (ламелярная) конформация (обычно в кристаллических полимерах) и т.д.
Рассмотрим одну изолированную цепь полимера, атомы углерода в которой связаны только s-связями. Предположим, что валентные углы в такой цепи не фиксированы и вращение вокруг s-связей является свободным. Такую модельную цепь называют свободно сочленённой (рис. 3.4 (1).Звенья свободно сочленённой цепи могут занимать в пространстве произвольные положения независимо от положения соседних звеньев. Подобная цепь может принимать любые конформации, т.е. является предельно гибкой.
В реальных цепях полимеров валентные углы имеют вполне определённую величину, и вращение звеньев происходит без их изменения (рис. 3.4(2)). Поэтому в реальной цепи звенья располагаются не произвольно: положение каждого последующего звена оказывается зависимым от положения предыдущего. Даже если предположить свободное вращение звеньев, то такая цепь может принимать меньшее число конформаций, чем свободно сочленённая. Но она способна сильно изгибаться из-за вращения звеньев. Молекулы, у которых наблюдаются достаточно интенсивные вращения звеньев вокруг s-связей, называют гибкоцепными , а полимеры со слабыми вращениями – жесткоцепными .Различают термодинамическую и кинетическую гибкость макромолекул.
Термодинамическая гибкость (равновесная гибкость) – способность макромолекул изменять свои конформации в результате внутримолекулярного теплового движения звеньев. Представим себе ситуацию, когда одна группа атомов цепи полимера получила в результате теплового движения звеньев некоторый импульс. Абсолютно жесткая молекула должна была бы под влиянием этого импульса переместиться целиком в новое положение в пространстве. В гибкой же макромолекуле перемещается только её определённый участок. Разные по величине импульсы, приложенные к разным участкам молекулы, приведут к перемещению различных по величине участков. Среднестатистический отрезок макромолекулы, перемещающийся как единое целое в элементарном акте теплового движения, называют сегментом (статистическим сегментом макромолекулы или статистическим элементом Куна). Чем жёстче цепь, т.е. чем больше активационный барьер вращения DU, тем больший отрезок цепи перемещается в элементарном акте теплового движения, т.е. тем больше по размерам сегмент. Таким образом, размер сегмента может служить мерой термодинамической гибкости макромолекул. Реальная молекула может быть представлена состоящей из N сегментов, каждый длиной А:
где L – длина цепи. У свободно сочленённой цепи А − длина звена, а у предельно жесткой макромолекулы А = L.
Представление о сегменте не является чисто формальным. Оказалось, что при измерении молярной массы полимера каким-либо физико-химическим методом, основанном на коллигативном свойстве (эбуллиоскопически, криоскопически, осмометрией и т.п.), получается, что она меньше истинной молярной массы, измеренной, например, вискозиметрическим методом, и равна молярной массе сегмента. Это означает, что макромолекулы в растворах ведут себя не как единое целое, а как совокупность малых молекул с длиной, равной длине сегмента А.
В качестве другой оценки термодинамической гибкости может служить отношение среднеквадратических размеров макромолекулы, свёрнутой в статистический клубок, к размерам, которые эта же молекула бы имела при абсолютно свободном вращении звеньев.
Кинетическая гибкость макромолекул – это способность макромолекул изменять свои конформации в результате воздействия внешних механических сил. В зависимости от соотношения энергии этих внешних воздействий и потенциального барьера вращения звеньев DU цепь полимера может в той или иной степени разворачиваться, т.е. проявлять кинетическую гибкость.
По аналогии с термодинамической гибкостью, в качестве меры кинетической гибкости может выступать длина кинетического сегмента. Действительно, если врезультате внешнего воздействия(например, мы потянули за концы полимерной ленты) одна группа атомов цепи полимера получит некоторый импульс, то в случае гибкой макромолекулы переместится только её определённый участок. Разные по величине импульсы, приложенные к разным участкам молекулы, приведут к перемещению различных по величине участков. Кинетический сегмент – это среднестатистический отрезок макромолекулы, перемещающийся как единое целое в элементарном акте внешнего воздействия. Чем короче сегмент, тем выше кинетическая гибкость макромолекулы.
Чаще всего в качестве меры кинетической гибкости принято рассматривать температуру стеклования – температурный интервал перехода полимера из стеклообразного в высокоэластическое состояние. Чем выше температура стеклования полимера, тем ниже кинетическая гибкость его макромолекул.
Универсальным и распространенным методом определения Т ст и Т т, а также исследования деформационных свойств полимеров является термомеханический метод. Метод состоит в измерении зависимости деформации e от температуры Т, графическое изображение этой зависимости называют термомеханической кривой (рис. 3.5).
Для аморфных линейных полимеров высокой молекулярной массы термомеханическая кривая имеет три участка, соответствующие трем физическим состояниям.
Первый участок (1) соответствует стеклообразному состоянию, для которого характерны малые деформации, второй (2) − высокоэластическому состоянию с большими обратимыми деформациями. На эти деформации накладывается (при длительном действии нагрузки) деформация течения, которая с повышением температуры увеличивается. При достаточно высоких температурах перемещения цепей как единого целого настолько облегчаются, что наступает истинное течение полимера. Полимер переходит в вязкотекучее состояние. Этот переход сопровождается резким увеличением деформации (участок 3).
Температуры Т ст и Т т соответствуют средним значениям интервалов температуры, при которых происходит переход от одного физического состояния полимера в другое.
В зависимости от свободного объема полимерное вещество находится в одном из физических состояний − стеклообразном, высокоэластическом, вязкотекучем. Переходы из одного состояния в другое происходят без выделения или поглощения теплоты. Температуры переходов называются температурами стеклования Т ст и текучести Т т.
Ниже Т ст межмолекулярное притяжение исключает повороты вокруг связей, однако оно недостаточно сильно, чтобы исключить такие повороты под действием внешней нагрузки.
Полимеры под нагрузкой проявляют низкую жесткость и ползучесть. Низкая жесткость является результатом обратимых поворотов вокруг связей и искажений углов между связями при кратковременном действии нагрузки. При длительном действии нагрузки деформация по сути является результатом необратимых поворотов вокруг связей и называется вынужденной высокоэластичной деформацией . Вытянутые молекулы представляют одну из разновидностей неравновесных структур.
Надмолекулярные структуры термопластов ниже Т ст зависят от условий обработки и охлаждения материала и обычно оказываются неравновесными. Сохранение неравновесных структур в изделиях является характерной особенностью термопластов. Получение одно- или двухосной ориентации в полимерных пленках используют для повышения прочности; полимерные волокна с ориентированной структурой образуют важную группу высокопрочных волокон.
Переход неравновесных структур в равновесные сопровождается короблением и усадкой изделий во время эксплуатации. Для уменьшения этого недостатка используют термическую стабилизацию - отжиг − при температурах, превышающих максимальные температуры эксплуатации.
Надмолекулярные структуры, в которых растягивающие напряжения от внешней нагрузки действуют вдоль валентных связей, отличаются большой жесткостью. Подобные структуры образуются после очень большой вытяжки полимерных волокон. Элементарная структурная единица волокна − фибрилла содержит чередующиеся кристаллические и аморфные участки. На аморфных участках молекулы предельно растянуты. Именно эти участки нагружаются при растяжении волокна, в результате чего модуль упругости (Е) оказывается очень большим. У обычного полиэтилена с аморфно-кристаллической структурой Е = 120 ... 260 МПа, у полипропилена Е = 160... 320 МПа. Сополимер этилена и пропилена при соотношении мономеров 1:1 не кристаллизуется и при температуре 20-25°С является каучуком, его модуль (при растяжении 300 %) всего 9-15 МПа. У полиэтиленового волокна в зависимости от технологии изготовления Е = 100 ... 170 ГПа (для сравнения у железа Е = 214 ГПа).
Физические свойства веществ зависят от их химического строения. Взаимосвязь между физическими свойствами полимеров и их строением очень сложна, является «опосредованной» и проявляется через влияние химического строения на гибкость макромолекулы.
Гибкость - одна из важнейших характеристик полимеров, определяющих его основные микроскопические свойства: высокоэластические, релаксационные и термомеханические свойства полимеров, а также особенности свойств их растворов. Гибкость характеризует способность макромолекул изменять свою форму под влиянием теплового движения звеньев или внешних механических воздействий.
Гибкость обусловлена внутренним вращением звеньев или частей макромолекул относительно друг друга.
Молекула любого вещества характеризуется определенным пространственным расположением атомов и наличием определенных связей между ними. Это обусловливает химическое строение (структуру, конфигурацию ) молекулы. Рассмотрим строение двух веществ - этана и этилена (рис. 6.1 ).
В молекуле этана атомы углерода связаны с атомами водорода и друг с другом ковалентными связями (формула" src="http://hi-edu.ru/e-books/xbook839/files/f122.gif" border="0" align="absmiddle" alt="-связь, вторая пара - пример">а и b ) схематически можно представить формулами
пример">пространственная изомерия (стереоизомерия) , обусловленная различным расположением заместителей относительно двойной связи. Этот вид пространственной изомерии получил название цис-транс-изомерии .
Отсутствие стереоизомеров в молекуле этана объясняется очень быстро происходящим вращением одних групп молекулы относительно других. Этот вид движения одной части молекулы относительно другой получил название внутреннего вращения .
В молекуле этана все атомы водорода равноценны, и поэтому можно предположить, что при любом их расположении в пространстве потенциальная энергия молекулы должна быть одной и той же, т.е. что вращение свободно. Однако в действительности внутреннее вращение в молекуле этана не свободно вследствие взаимодействия между химически не связанными друг с другом соседними атомами.
При тепловом движении непрерывно изменяется пространственное расположение атомов. Каждому положению атомов соответствует определенное значение потенциальной энергии молекулы, которая определяется взаимодействиями между атомами, электронами, ядрами и т.д.
При повороте группы пример">этана вокруг линии, соединяющей атомы углерода, изменяется потенциальная энергия U .
Графически различные крайние расположения атомов в молекуле можно представить в виде проекций молекулы на горизонтальную плоскость (pис. 6.2 ).
Предположим, что при расположении атомов в молекуле этана так, как показано на рис. 6.2 , а, потенциальная энергия молекулы равна формула" src="http://hi-edu.ru/e-books/xbook839/files/f125.gif" border="0" align="absmiddle" alt=" должна повернуться относительно другой на 60° (рис. 6.2 , б)..gif" border="0" align="absmiddle" alt=" на 60° молекула снова возвращается в положение (рис. 6.2 , а).
Из рассмотрения этого примера, очевидно, что выделение">рис. 6.2 , б, потому что в этом случае между ними проявляются силы отталкивания, стремящиеся перевести эти атомы в наиболее энергетически выгодное, устойчивое положение, изображенное на рис. 6.2 , а. Если принять потенциальную энергию молекулы при расположении атомов, показанном на рис. 6.2 , а, равной 0, то потенциальная энергия, соответствующая модели, приведенной на рис. 6.2 , б, имеет максимальное значение.
Энергия, необходимая для перехода молекулы из положения с минимальным значением потенциальной энергии в положение, соответствующее ее максимальному значению, называется потенциальным или активационным барьером вращения .
Для молекулы этана потенциальный барьер вращения сравнительно невелик, и при комнатной температуре кинетической энергии достаточно для осуществления свободного вращения. Поэтому этан фактически представляет собой смесь молекул, атомы которых могут занимать различное пространственное положение, т.е. является смесью поворотных изомеров. Переход из одного положения в другое осуществляется 10 раз в секунду, т.е. очень быстро, поэтому выделить молекулы этана с разным расположением атомов практически невозможно. Однако спектроскопическими методами можно доказать реальность их существования.
Повышенные значения потенциального барьера вращения наблюдаются при увеличении числа групп пример">бутан и бутилен ). Потенциальные барьеры вращения вокруг связей С-О, С-S, С-Si сравнительно невелики.
Если потенциальные барьеры достаточно велики, то даже в случае насыщенных соединений можно выделить молекулы с определенной пространственной структурой.
Вокруг двойной связи также может происходить вращение отдельных групп, но для этого необходимо разорвать формула" src="http://hi-edu.ru/e-books/xbook839/files/f122.gif" border="0" align="absmiddle" alt="-связями. Звенья такой цепи находятся в тепловом движении, т.е. одно звено может вращаться относительно соседнего звена. Предположим, что валентные углы в такой цепи не фиксированы и вращение вокруг выделение">свободно сочлененной .
Очевидно, что звенья свободно сочлененной цепи могут занимать в пространстве произвольные положения независимо от положения соседних звеньев. Такая цепь может принимать любые конформации, т.е. является предельно гибкой (рис. 6.3 ). В реальных цепных молекулах полимеров валентные углы имеют вполне определенную величину, и вращение звеньев происходит без изменения валентного угла (см. рис. 6.4 ). Поэтому в реальной цепи звенья располагаются не произвольно, а положение каждого последующего звена оказывается зависимым от положения предыдущего. Даже если предположить наличие свободного вращения, такая цепь принимает меньшее число конформации, чем свободно сочлененная цепь, но она также способна сильно изгибаться.
В реальных системах молекулы полимеров окружены другими себе подобными молекулами и между ними всегда существует межмолекулярное взаимодействие, которое оказывает влияние на степень заторможенности вращения. Поскольку учет этого взаимодействия очень сложен, для количественных расчетов ограничиваются учетом только внутримолекулярного взаимодействия химически не связанных между собой атомов и групп атомов одной и той же молекулы полимера.
Повороты звеньев и переход их от расположения, соответствующего одному минимуму энергии, к расположению, соответствующему другому минимуму энергии, могут происходить только при наличии необходимого запаса энергии.
Если молекула имеет запас энергии меньший опред-е">колебание атомов относительно положения минимальной энергии - это ограниченное или заторможенное вращение . Чем интенсивнее эти колебания, тем молекула более гибка. Таким образом, реальная цепь полимера вследствие внутримолекулярного взаимодействия принимает меньшее число конформаций, чем свободно сочлененная цепь.
Полимеры, у которых наблюдаются достаточно интенсивные крутильные колебания, называются гибкоцепными , а полимеры, у которых повороты одной части цепи относительно другой затруднены, - жесткоцепными .
Различают два понятия гибкости цепи - ТДГ - термодинамическую гибкость и КГ - кинетическую гибкость цепи полимеров .
ТДГ определяет способность цепи к конформационным превращениям (т.е. без разрыва химических связей под действием теплового движения).
Это равновесная гибкость, которая реализуется в очень разбавленных растворах, в которых цепи находятся в изолированном состоянии.
ТДГ характеризуется несколькими параметрами. Например, параметр жесткости формула" src="http://hi-edu.ru/e-books/xbook839/files/f130.gif" border="0" align="absmiddle" alt=" - параметр оценки гибкости цепных ММ, гибкость которых вызвана вращением вокруг валентных связей без деформации валентных углов. Для многих полимеров это невозможно.
Наиболее универсальной мерой оценки гибкости является величина сегмента Куна - статистического элемента (или отрезка цепи) длиной А, положение которого не зависит от положения соседних элементов или отрезков.
Реальную цепь макромолекулы можно разбить на N независимых статистических элементов отрезков А.
В свободно сочлененной цепи положение каждого звена не зависит от положения предыдущего, т.е. отсутствует корреляция в расположении звеньев. В реальной цепи положения звеньев в пространстве взаимосвязаны. Однако при очень большой длине цепи между направлениями расположения звеньев, достаточно удаленных друг от друга, корреляция также отсутствует.если такие звенья соединить линиями (рис. 6.5 ), то направления этих линий оказываются независимыми. Это означает, что реальную цепь, состоящую из n повторяющихся звеньев (длина каждого звена l), можно разбить на N независимых статистических элементов (отрезков, или сегментов) длиной А .
ТД сегмент - в общем случае не отрезок реальной цепи, а эквивалентная величина , отражающая интенсивность колебательного движения звеньев или гибкость цепи.
Для предельно гибкой цепи А = l звена..gif" border="0" align="absmiddle" alt=" можно вычислить по количеству сегментов М = N сегментов * А (молярная масса звекна).
В табл. 6.1. приведены величины сегментов Куна некоторых образцов полимеров.
Таблица 6.1
Показатели, характеризующие ТДГ цепи
Полимер |
Звено |
А, нм |
Число |
Конформация |
| Полиэтилен | СН 2 -СН 2 - |
Статист. клубок |
||
| Полистирол | СН 2 -СНС 6 Н 5 - |
Статист. клубок |
||
| ПВХ | СН 2 -СНCl- |
Статист. клубок |
||
| Полиметил-метакрилат | СН 2 -С(СН 3)СООСН 3 - |
Статист. клубок |
||
| ЭтилЦл | Статист. клубок |
|||
| Поли-n-бензамид | NH- С 6 Н 5 -CO- |
Коленчатый вал |
||
| Биополимеры |
Природа заместителей мало влияет на ТДГ. Наибольшая жесткость у полимера с полярными группами, близко расположенными. Циклические полиацетали (Цл, и производные) относятся к полужестким полимерам.
Кинетическая гибкость (КГ) характеризует скорость перехода из одного конформационного положения в другое.
Скорость конформационных превращений зависит от соотношения величин потенциального барьера вращения и энергии внешних воздействий (тепловых, механических и др.).
КГ характеризуется величиной кинетического сегмента , т.е. той части ММ, которая отзывается на внешнее воздействие как единое целое.
Кинетический сегмент (в отличие от ТДС) - величина, которая зависит от Т и силы воздействия.
Рассмотрим различия между ТДГ и КГ (рис. 6.6 ).
У полимеров вследствие внутри- и межмолекулярных взаимодействий зависимость формула" src="http://hi-edu.ru/e-books/xbook839/files/f126.gif" border="0" align="absmiddle" alt=".gif" border="0" align="absmiddle" alt=". Разность энергий перехода выделение">термодинамическую гибкость . Она определяет способность цепи изгибаться под влиянием теплового движения.
Другой характеристикой гибкости является скорость перехода звеньев из одного положения в другое..gif" border="0" align="absmiddle" alt=", тем медленнее повороты звеньев и меньше гибкость. Гибкость макромолекул, определяемая величиной выделение">кинетической гибкостью ., густоту пространственной сетки, размер заместителей и температуру.
Карбоцепные полимеры
У карбоцепных полимеров наименее полярными являются предельные углеводороды..gif" border="0" align="absmiddle" alt=", следовательно полимеры обладают большой кинетической и термодинамической гибкостью .
Примеры: ПЭ, ПП, ПИБ.
Особенно низки значения формула" src="http://hi-edu.ru/e-books/xbook839/files/f134.gif" border="0" align="absmiddle" alt="Полибутадиен
Введение в макромолекулы заместителей , содержащих полярные группы приводит к внутри- и межмолекулярным взаимодействиям. При этом существенно влияют степень полярности групп и симметричность их расположения.
Пример:
Наиболее полярные группы формула" src="http://hi-edu.ru/e-books/xbook839/files/f136.gif" border="0" align="absmiddle" alt="
При введении полярных групп возможны три случая по влиянию на гибкость:
Опред-е">Гетероцепные полимеры
У гетероцепных полимеров вращение возможно вокруг связей С-О, С-N, Si-O, C-C. Значения пример"> полиэфиры, полиамиды, полиуретаны, силоксановые каучуки .
Однако гибкость гетероцепных полимеров может ограничиваться межмолекулярными взаимодействиями за счёт образования Н-связей (например, у целлюлозы, полиамидов ). Целлюлоза (Цл) является одним из жесткоцепных полимеров . У неё содержится большое количество полярных групп (-OH) и поэтому для целлюлозы характерны внутри- и межмолекулярные взаимодействия и высокие значения опред-е">Молекулярная масса полимера
Увеличение формула" src="http://hi-edu.ru/e-books/xbook839/files/f4.gif" border="0" align="absmiddle" alt=" возрастает число конформаций, которое может принимать макромолекула и гибкость цепей увеличивается и даже при больших опред-е">Густота пространственной сетки
Чем больше химических связей между макромолекулами, тем меньше гибкость цепей, т.е. с увеличением густоты пространственной сетки гибкость уменьшается.
При этом при малом числе связей (2-3% S) гибкость вулканизированного каучука формула" src="http://hi-edu.ru/e-books/xbook839/files/f144.gif" border="0" align="absmiddle" alt=" Кг (эбонит - каучук с 30% S).
Влияние размера и количества заместителей
Увеличение числа полярных и больших по размеру заместителей снижает подвижность звеньев макромолекулы и уменьшает кинетическую гибкость.
Примером является снижение гибкости макромолекул сополимера бутадиена и стирола при увеличении содержания громоздких фенильных заместителей в цепи.
ПС при комнатных Т не изменяет конформаций, т.е. является жестким полимером.
Если при одном атоме углерода в основной цепи полимера имеются два заместителя (например, формула" src="http://hi-edu.ru/e-books/xbook839/files/f140.gif" border="0" align="absmiddle" alt=" в звеньях ПММА), то макромолекула становится кинетически жесткой.
Температура
С повышением температуры возрастает кинетическая энергия макромолекулы..gif" border="0" align="absmiddle" alt=", звенья начинают вращаться.
С повышением температуры величина мало изменяется, а скорость поворота звеньев увеличивается и кинетическая гибкость возрастает.
Пример: ПС при 100°С - гибкий полимер.
1. Особенности строения полимеров. Причины гибкости макромолекул. Образование ассоциатов
Высокомолекулярными соединениями называют вещества, имеющие относительную молекулярную массу приблизительно от 10000 до нескольких миллионов. ВМС, состоящие из большого числа повторяющихся одинаковых звеньев, называются полимерами.
Молекулы полимеров могут быть линейными и разветвленными. Именно линейные формы макромолекул определяют типичные свойства полимеров: каучукоподобная эластичность, способность образовывать прочностные пленки и нити, набухать, давать при растворении вязкие растворы.
Разветвление у макромолекул сильно влияет на их гибкость. Короткие и часто расположенные боковые цепи увеличивают жесткость молекул. На гибкость макромолекулы могут влиять молекулы растворителя или пластификаторы.
Гибкость углеводородной цепи обуславливается вращением одних участков цепи относительно других вокруг одинаковой валентной связи, соединяющей соседние атомы углерода. Так как таких отдельных связей в макромолекуле множество, то становится понятной та исключительная гибкость, которой обладают углеводородные цепочки. Молекулы полимеров не связанные друг с другом и ведут себя вполне самостоятельно, когда они находятся в относительно разбавленных растворах. В концентрированных растворах, когда вероятность столкновения молекул растворенного вещества велика, макромолекулы могут взаимодействовать и образовывать ассоциаты.
Ассоциаты в разбавленных растворах полимеров не являются постоянно существующими образованиями и не имеют определенного состава. Ассоциаты образуются и в растворах НМС за счет столкновения двух, трех, четырех и более молекул. Особенностью образования ассоциатов в растворах ВМС является то, что длинные и гибкие макромолекулы могут входить отдельными своими участками в состав различных ассоциатов.
2. Общие и отличительные свойства растворов высокомолекулярных соединений (ВМС) и золей
Растворы ВМС представляют собой истинные растворы, термодинамически устойчивые и обратимые, не нуждающиеся в стабилизаторе частицы, содержащиеся в таких растворах, состоят не из множеств малых молекул, как это имеет место у коллоидов, и представляют отдельные молекулы относительно очень больших размеров. В этом и заключается отличие растворов ВМС от растворов низкомолекулярных соединений.
Растворы ВМС в плохих растворителях содержат молекулы свернутые в компактный клубок с явно выраженной межфазной поверхностью.
Они представляют отдельную фазу. Такие растворы ВМС можно отнести к коллоидным системам. Растворы ВМС благодаря большим размерам их молекул обладают рядом свойств лиозолей, что позволяет рассматривать многие проблемы одновременно и для коллоидных растворов и для растворов ВМС.
В отличие от золей, для растворов ВМС характерны большая вязкость, высокая устойчивость, способность к набуханию.
Золи могут существовать в газообразном состоянии (аэрозоли), а ВМС – нет, т.к. произойдет разрыв макромолекулы.
3. Набухание. Стадии процесса набухания. Факторы, влияющие на набухание. Кинетика набухания. Степень набухания. Ограниченное и неограниченное набухание. Давление набухания. Концентрация
Растворение высокомолекулярных соединений с линейными гибкими молекулами в отличие от растворения НМС сопровождается набуханием.
При набухании высокомолекулярных соединений поглощает низкомолекулярный растворитель, значительно увеличивается в массе, при этом изменяет механические свойства без потери однородности. Объем ВМС может увеличиваться при набухании до 1000 – 1500%.
На первой стадии набухания происходит сольватация макромолекул в результате диффузии растворителя в высокомолекулярное вещество. Эта стадия характеризуется выделением тепла и упорядочением расположения молекул растворителя около макромолекулы, в результате чего энтропия системы в первой стадии растворения обычно даже понижается. Основное значение этой стадии при растворении сводится к разрушению связей между отдельными макромолекулами, следствии чего они становятся свободными.
Второй стадией является набухание или растворение, обусловленное чисто энтропийными причинами. В этой стадии, поскольку сольватация уже завершилась, тепловой эффект равен нулю или имеет отрицательное значение, а энтропия резко возрастает. Вторую стадию растворения можно рассматривать как чисто осмотический процесс. Легче всего набухают полимеры в вязкотекучем и высокоэластичном состоянии.
К факторам, влияющим на набухание, относятся: термодинамическая активность растворителя, температура, физическое состояние полимера, природа полимера и растворителя. Типичные кинетические кривые набухания, характеризующие зависимость растворителя, представлены на рисунке.
Кинетические кривые для ограниченного набухания представляют аналитически:
![]() ,
,
где - константа скорости набухания; - степень набухания при достижении равновесия и ко времени соответственно.
Проинтегрировав, получим уравнение кинетики набухания, подобное уравнению для кинетики ленгмюровской адсорбции:
![]() ,
,
Набухание полимера в жидкости характеризуется степенью набухания , вычисляемой по формуле:
где - навеска полимера до и после набухания.
Набухание не всегда заканчивается растворением. Очень часто после достижения известной степени набухания процесс прекращается.
Причины ограниченного набухания:
1. ВМС и растворитель способны смешиваться ограниченно. Поэтому в результате набухания в системе образуется две фазы – насыщенный раствор полимера в растворителе и насыщенный раствор растворителя в полимере (гель, студень). Такое ограниченное набухание носит равновесный характер.
... «мицелла» и «мицеллярный раствор». Эти термины были использованы им для обозначения систем, образованных нестехиометрическими соединениями в водной среде. Основная заслуга в становлении коллоидной химии как науки принадлежит Т. Грэму. Как уже отмечалось выше, именно этому ученому принадлежит идея введения термина «коллоид», производного от греческого слова «kolla», обозначающего «клей». Занимаясь...





Расстояние, пройденное веществом по сорбенту, прямо пропорционально растворимости данного вещества в пропускаемом растворителе. Даёт возможность полностью разделять вещества, входящие в состав разделяемой смеси. Коллоидная химия Дисперсные системы – это системы, состоящие из множества частиц одной фазы (дисперсной), распределённых в объёме другой фазы – дисперсионной. Дисперсионная среда...





И многое другое, без чего немыслима сама жизнь. Все человеческое тело – это мир частиц, находящихся в постоянном движении строго по определенным правилам, подчиняющимся физиологии человека. Коллоидные системы организмов обладают рядом биологических свойств, характеризующих то или иное коллоидное состояние: 2.2 Коллоидная система клеток. С точки зрения коллоидно-химической физиологии...
Металлов с белками, нуклеиновыми кислотами, липидами. Её практическое применение связано с синтезом фарамакологических препаратов, действие которых обусловленно комплексными ионами металлов. Биоорганическая Химия Изучает связь между строениями органических веществ и их биологическими функциями, использующих в основном методы органической и физической химии, а также физики и математики. ...